
| A. | 铜是一种紫红色金属 | |
| B. | 铜是热和电的良导体 | |
| C. | 铜是人类使用最早、应用最广泛的金属之一 | |
| D. | 铜在自然界中主要以单质的形式存在 |
分析 铜是金属,具有金属的通性,导电、导热、延展性,是一种紫红色金属,自然界中铜以化合态和游离态两种形式存在,铜的化学性质不活泼,金属大规模被使用的先后顺序跟金属的活动性关系最大,金属活动性较弱时,比较难形成化合物,常以单质形式存在,比较容易被利用,金属的活动性越强,就越难把它制成单质,所以在科技不发达的时候,难以被利用;另外,金属能否被广泛应用,还与它们在地壳中的含量有关,含量越大,越容易被发现.
解答 解:A、铜呈紫红色光泽的金属,一种紫红色金属,故A正确;
B、铜是金属,具有金属的通性,导电、导热、延展性,铜是热和电的良导体,故B正确;
C、由于铜的活动性比较弱,以单质形式存在的比较多,在我国,距今4000年前的夏朝已经开始使用红铜,即天然铜,铜是人类使用最早、应用最广泛的金属之一,故C正确;
D、自然界中铜主要以化合态形式存在,故D错误;
故选D.
点评 本题考查了铜性质的分析应用,掌握基础是关键,题目较简单.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
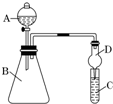 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
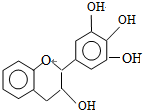
| A. | 分子式为C15H12O5 | |
| B. | 1molEGC与5molNaOH恰好完全反应 | |
| C. | 易发生氧化反应和取代反应,不能发生消去反应 | |
| D. | 遇FeCl3溶液能发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内混合气体的密度不随时间的变化而变化 | |
| B. | 单位时间内每消耗3mol H2,同时生成2mol NH3 | |
| C. | 混合气体的总质量不随时间的变化而变化 | |
| D. | 混合气体的总物质的量不随时间的变化而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
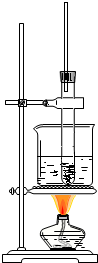 硝基苯是制造染料的重要原料.某同学在实验室里用右图装置制取硝基苯,主要步骤如下:
硝基苯是制造染料的重要原料.某同学在实验室里用右图装置制取硝基苯,主要步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 电负性 离子半径 键的极性 | 熔点 |
| N<O O2->Al3+ C-H<H-O | Al<Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和苯酚均无毒,但都能用于消毒、杀菌 | |
| B. | 乙醇和苯酚均能和金属Na反应置换出氢气 | |
| C. | 苯酚能与甲醛反应制造酚醛树脂 | |
| D. | 乙醇的沸点比乙烷高是因为乙醇分子间可以形成氢键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com