
 ij��ѧ�о���ѧϰС��Ϊ�˽�ӹ�ҵ�����ᴿ��ķ������������й����ϣ�Br2�ķе�Ϊ59�棬����ˮ���ж��Ժ�ǿ��ʴ�ԣ����Dzι��������̺���װ����ͼװ�ü�ͼ��
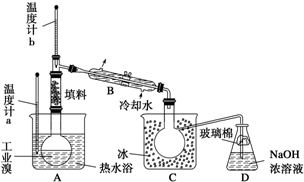
ij��ѧ�о���ѧϰС��Ϊ�˽�ӹ�ҵ�����ᴿ��ķ������������й����ϣ�Br2�ķе�Ϊ59�棬����ˮ���ж��Ժ�ǿ��ʴ�ԣ����Dzι��������̺���װ����ͼװ�ü�ͼ������ ��1����ͼ��֪���������ƣ�
��2������������ԣ��ɸ�ʴ��
��3��ͨ���¶ȼƿ��ƺ�Br2���ڵ��¶ȣ�
��4��Br2�ķе�Ϊ59�棬C����ȴ�ռ�Һ�壻
��5��������NaBr��Ӧ�����壬�岻������ˮ���������л��ܼ�������е�ͣ���
��6�����ж����һӷ��������ŷ��ڻ����У�
��� �⣺��1����ͼ��֪����B�������ܣ��ʴ�Ϊ�������ܣ�
��2������и�ʴ�ԣ����Ը�ʴ�����Բ������ܺ��������ʴ�Ϊ��Br2��ʴ��
��3�������Ŀ�ģ�����ͨ���е㲻ͬ���ᴿBr2������Ҫͨ���¶ȼƿ��ƺ�Br2���ڵ��¶ȣ�������ʹBr2������
�ʴ�Ϊ�������¶ȼ�b���¶ȣ����ռ�59��ʱ����֣�
��4��C��Բ����ƿ�в���Һ����ɫΪ�����ɫ���ñ���ȴ��Ŀ���������壬��ֹ��ӷ���
�ʴ�Ϊ�������ɫ�������壬��ֹ��ӷ���
��5��Ϊ��ȥ�ò������Բ���������Cl2���������м���NaBr��Һ����ַ�Ӧ���������ʵ��ܽ��Ի�е㲻ͬ�����÷�Һ������ķ������룬
�ʴ�Ϊ����Һ��������
��6��Br2�ж��������ŷ��ڻ����У�D��ŨNaOH��Һ�����������ջӷ������壬�ʴ�Ϊ�����ջӷ������壮
���� ���⿼����������ᴿ���ۺ�Ӧ�ã�Ϊ��Ƶ���㣬����ʵ��װ�õ����á����ʵ����ʡ�ʵ�鼼��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬��Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�¶�/�� ʱ��/min | 0 | 10 | 20 | 40 | 50 |
| T1 | 1.2 | 0.9 | 0.7 | 0.4 | 0.4 |
| T2 | 1.2 | 0.8 | 0.56 | �� | 0.5 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ɹ㷺����ʳƷ������ | |
| B�� | ����ϩ������Ʒ������ʳƷ�İ�װ | |
| C�� | ����������Һ�����ڻ���������ɱ�� | |
| D�� | ��������ұ����������ԭ�ϣ�Ҳ��һ�ֽϺõ��ͻ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaAlO2��Һ��ͨ�����CO2��AlO2-+CO2+2H2O�TAl��OH��3��+HCO3- | |
| B�� | ��������Һ�������Һ��ϣ�SiO32-+2H+�TH2SiO3�� | |
| C�� | MnO2��Ũ���ᷴӦ��Cl2��MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2Cl-+Cl2��+2H2O | |
| D�� | Ũ�����м���������۲����ȣ�Fe+3NO3-+6H+$\frac{\underline{\;\;��\;\;}}{\;}$Fe3++3NO2��+3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��100 mL����ƿ����50 mL 0.1 mol/L���� | |
| B�� | ��������ƽ�ϳ���NaOHʱ��Ӧ��NaOH�������С�ձ��г��� | |
| C�� | ��25 mL��Ͳ��ȡ4.0 mol/L������5.62 mL | |
| D�� | ��������ƽȷ��ȡ5.85 g NaCl���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� �� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | N | O | F | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com