
| A、气态氢化物的稳定性:B<E |
| B、最高价氧化物对应的水化物碱性:C<D |
| C、简单离子半径:E<D |
| D、均含有A,B,C,E四种元素形成的两种化合物可以相互反应 |


科目:高中化学 来源: 题型:
| A、0.1mol?L-1某二元弱酸酸式盐NaHA溶液中:c(Na+)=c(A2-)+c(HA-)+c(H2A) |
| B、向NH4HSO4溶液中加入等物质的量的NaOH形成的溶液中:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| C、0.1 mol?L-1的Na2CO3溶液中:c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) |
| D、25℃时,pH=9.4、浓度相同的HCN与NaCN的混合溶液中:c(Na+)>c(CN-)>c(HCN)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、只有①② |
| C、只有②③④ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、容器I、Ⅲ中平衡常数相同 |
| B、容器Ⅱ、Ⅲ中正反应速率相同 |
| C、容器Ⅱ、Ⅲ中的反应达平衡时,SO3的体积分数:Ⅱ>Ⅲ |
| D、容器 I中SO2的转化率与容器 II中SO3的转化率之和小于1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
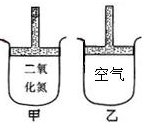 常温常压下在带有可移动活塞的甲、乙容器(如图)里分別充有二氧化氮和空气.现分別进行下列两个实验:
常温常压下在带有可移动活塞的甲、乙容器(如图)里分別充有二氧化氮和空气.现分別进行下列两个实验:| A、①甲>乙 ②甲>乙 |
| B、①甲>乙 ②甲<乙 |
| C、①甲<乙 ②甲<乙 |
| D、①甲>乙 ②甲=乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④ | B、①②④ |
| C、②③⑤ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下,1.5 mol H2和0.5 mol N2充分反应后,可得到NH3的分子数为NA |
| B、常温常压下,18 g H2O中含有的电子总数为8NA |
| C、足量的Cu与Cl2反应生成0.2 mol产物时,失去的电子数为0.4NA |
| D、标准状况下,22.4 L己烯中含有的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油裂化得到的汽油是纯净物 |
| B、天然气是一种较为清洁的化石燃料 |
| C、石油产品都可用于聚合反应 |
| D、水煤气是指煤气中含有一定量的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.l mol?L-1的氨水溶液中:Na+、NH4+、NO3-、CO32- |
| B、0.1 mol?L-1的盐酸溶液中:K+、[Ag(NH3)2]+、Cl-、NO3- |
| C、使蓝色石蕊试纸变红的溶液中:CO32-、SO32-、Na+、K+ |
| D、由永电离出的c(H+)=1×l0-12 mol?L-l的溶液中:Fe2+、ClO-、K+、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com