
下列物质的水溶液在蒸发皿中加热蒸干灼烧,能得到原物质的是
①NaAlO2 ②FeCl3 ③硫酸铝 ④绿矾 ⑤高锰酸钾 ⑥硝酸银⑦碳酸氢钙 ⑧MgCl2 ⑨Na2SO3 ⑩CaCl2
A、①③⑤⑥⑧⑩ B、②③④⑤⑨⑩
C、③⑤⑦⑩ D、①③⑩
科目:高中化学 来源:2014-2015陕西省宝鸡市高二上学期期末化学试卷(解析版) 题型:选择题
二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是
A.利用金属钠或者金属钾 B.利用质谱法
C.利用红外光谱法 D.利用核磁共振氢谱
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省潍坊市高一上学期1月月考化学试卷(解析版) 题型:选择题
除去下列括号内杂质的试剂或方法错误的是
A.HNO3溶液(H2SO4),适量BaCl2溶液,过滤
B.Fe2+(Fe3+),还原铁粉,过滤
C.Cl2(HCl),饱和食盐水,洗气
D.CO2(SO2),饱和NaHCO3溶液,洗气
查看答案和解析>>
科目:高中化学 来源:2014-2015河南周口中英文学校上期高二第三次考试化学试卷(解析版) 题型:填空题
(10分)一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:
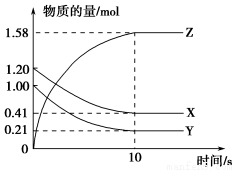
(1)从反应开始到10 s,用Z表示的反应速率为________________________。
X的物质的量浓度减少了____________,Y的转化率为_________________。
(2)该反应的化学方程式为____________________________________。
(3)10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示:
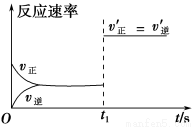
则下列说法符合该图像的是________。
A.t1时刻,增大了X的浓度
B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积
D.t1时刻,使用了催化剂
查看答案和解析>>
科目:高中化学 来源:2014-2015河南周口中英文学校上期高二第三次考试化学试卷(解析版) 题型:选择题
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图所示从下表中选出正确选项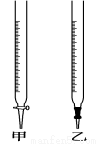
选项 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 |
A | 碱 | 酸 | 石蕊 | 甲 |
B | 酸 | 碱 | 酚酞 | 甲 |
C | 碱 | 酸 | 甲基橙 | 乙 |
D | 酸 | 碱 | 酚酞 | 乙 |
查看答案和解析>>
科目:高中化学 来源:2014-2015重庆市高二上学期第三次月考化学试卷(解析版) 题型:实验题
某学生试图用电解法根据电极上析出物质的质量来验证阿伏加德罗常数数值,其实验方案的要点为:①用直流电源电解CuCl2溶液,所用仪器如下图所示。②在电流强度为I A,通电时间为t min后,精确测得电极上析出铜的质量为m g。
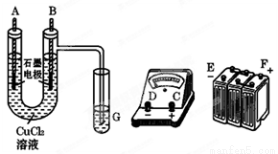
试回答:(1)连接这些仪器的正确顺序为(用图中标注仪器接线柱的英文字母表示):
E接 ,C接 , 接F。
(2)写出B电极上发生的电极反应式: ;
G试管中淀粉KI溶液变化的现象为 ,
相应的离子方程式是 。
(3)为精确测定电极上析出的铜的质量,所必需的实验步骤的先后顺序应是 。(选填下列操作步骤的编号)
①称量电解前电极质量
②刮下电解后电极上的铜并清洗
③用蒸馏水清洗电解后的电极
④低温烘干电极后称量
⑤低温烘干刮下的铜后称量
⑥再次低温烘干后称量至恒重
(4)已知电子的电量为1.6×10-19C。试列出阿伏加德罗常数的计算式:NA= 。
查看答案和解析>>
科目:高中化学 来源:2014-2015重庆市高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列关于电解质溶液的叙述不正确的是
A.常温下,pH=7的CH3COONa与CH3COOH的混合溶液中离子浓度大小顺序为c(Na+)=c(CH3COO-)>c(H+)= c(OH-)
B.将pH=10的氨水稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量前者小于后者
D.常温下,同浓度的Na2CO3溶液与NaHCO3溶液相比,Na2CO3溶液的pH较大
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省赣州市北校区高一12月月考化学试卷(解析版) 题型:填空题
(8分)(1)向某溶液中加入KSCN溶液无明显现象,再滴入数滴氯水后,溶液立即变成红色,则原溶液中一定含有________离子,要除去FeCl3溶液中少量的氯化亚铁,可行的办法是________(填字母)。
A.加入铜粉 B.加入铁粉 C.通入氯气 D.加入KSCN溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式
________________________ _______。
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式____________ __________________________。
(3)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是_________,区别该液体和FeCl3溶液可用 方法。
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列溶液硝酸根离子的物质的量浓度与50ml 1 mol·L-1硝酸铝溶液中硝酸根离子的物质的量浓度相等的是
A.150 ml、1 mol·L-1 硝酸钠溶液 B.75 ml、2.5 mol·L-1 硝酸钙溶液
C.150 ml、3 mol·L-1 硝酸钾溶液 D.50 ml、3 mol·L-1 硝酸镁溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com