
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 合成氨的原理为:N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol,该反应的能量变化如图所示.
合成氨的原理为:N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol,该反应的能量变化如图所示.| 7 |
| 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
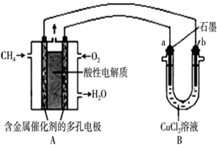 如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图:
如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔点:CO2>KCl>SiO2 |
| B、沸点:HF>HBr>HI |
| C、热稳定性:PH3<H2S<HCl |
| D、硬度:铝>镁>铝镁合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化合物 | 燃烧热 | 化合物 | 燃烧热 |
| 甲烷 | 891.0 | 正丁烷 | 2 878.0 |
| 乙烷 | 1 560.8 | 异丁烷 | 2 869.6 |
| 丙烷 | 2 221.5 | 2甲基丁烷 | 3 531.3 |
| A、热稳定性:正丁烷>异丁烷 |
| B、乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=-1 560.8 kJ/mol |
| C、正戊烷的燃烧热大于3 531.3 kJ/mol |
| D、相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com