
·ÖĪö £Ø1£©¢ŁHClŅ×ČÜÓŚĖ®£»
¢ŚĖ®ŗĶĘūÓĶ»„²»ĻąČÜ£»
¢ŪĖÄĀČ»ÆĢ¼ŗĶ¼×±½µÄ·Šµć²»Ķ¬£»
¢ÜÓĆŹ³ÓĆ¾Ę¾«½žÅŻÖŠ²ŻŅ©ĪŖŻĶČ”²Ł×÷£»
¢ŻĻõĖį¼ŲŗĶĀČ»ÆÄʵÄČܽā¶ČĖęĪĀ¶ČµÄ±ä»Æ²»Ķ¬£»
£Ø2£©A£®²»Ņ»¶ØÉś³ÉAgCl³Įµķ£»
B£®²»Ņ»¶ØÉś³ÉĮņĖį±µ³Įµķ£»
C£®Ą¶É«³ĮµķĪŖĒāŃõ»ÆĶ£»
D£®æÉÄÜÉś³É¹čĖį³Įµķ£»
E£®AgCl²»ČÜÓŚĻõĖį£»
F£®ĻõĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬ČÜŅŗÖŠæÉÄÜŗ¬ÓŠSO32-£»
G£®æÉÄÜÉś³ÉAgCl³Įµķ£»
H£®¼ÓČėŃĪĖįĖį»Æ£¬ÓŠĪŽÉ«ĪŽĪ¶ĘųĢå²śÉś£¬ČÜŅŗÖŠæÉÄÜŗ¬ÓŠHCO3-£»
£Ø3£©¢ŁĻņBa£ØHCO3£©2ČÜŅŗÖŠµĪČėNaHSO4ČÜŅŗ£¬ÖĮBa2+øÕŗĆ³ĮµķĶźČ«£¬·“Ӧɜ³ÉBaSO4”¢H2O”¢CO2£»
¢ŚĻņBa£ØOH£©2ČÜŅŗÖŠµĪČėNaHSO4ČÜŅŗ£¬ÖĮøÕŗĆÖŠŗĶĶźČ«£¬¶žÕß°“ĪļÖŹµÄĮæ±ČÖµ1£ŗ2·“Ó¦£®
½ā“š ½ā£ŗ£Ø1£©¢ŁHClŅ×ČÜÓŚĖ®£¬æÉÓĆĻ“ĘųµÄ·½·Ø·ÖĄė£¬¹Ź“š°øĪŖ£ŗF£»
¢ŚĖ®ŗĶĘūÓĶ»„²»ĻąČÜ£¬æÉÓĆ·ÖŅŗµÄ·½·Ø·ÖĄė£¬¹Ź“š°øĪŖ£ŗC£»
¢ŪĖÄĀČ»ÆĢ¼ŗĶ¼×±½µÄ·Šµć²»Ķ¬£¬æÉÓĆÕōĮóµÄ·½·Ø·ÖĄė£¬¹Ź“š°øĪŖ£ŗD£»
¢ÜÓĆŹ³ÓĆ¾Ę¾«½žÅŻÖŠ²ŻŅ©ĪŖŻĶČ”²Ł×÷£¬¹Ź“š°øĪŖ£ŗA£»
¢ŻĻõĖį¼ŲŗĶĀČ»ÆÄʵÄČܽā¶ČĖęĪĀ¶ČµÄ±ä»Æ²»Ķ¬£¬æÉÓĆ½į¾§·Ø·ÖĄė£¬¹Ź“š°øĪŖ£ŗB£»
£Ø2£©A£®²»Ņ»¶ØÉś³ÉAgCl³Įµķ£¬Ó¦ĻČ¼ÓČėĻõĖįĖį»Æ£¬¹ŹA“ķĪó£»
B£®²»Ņ»¶ØÉś³ÉĮņĖį±µ³Įµķ£¬Ó¦ĻČ¼ÓČėŃĪĖį£¬ŌŁ¼ÓČėĀČ»Æ±µ£¬¹ŹB“ķĪó£»
C£®Ą¶É«³ĮµķĪŖĒāŃõ»ÆĶ£¬æÉĖµĆ÷ŌČÜŅŗÖŠÓŠCu2+£¬¹ŹCÕżČ·£»
D£®æÉÄÜÉś³É¹čĖį³Įµķ£¬¹ŹD“ķĪó£»
E£®AgCl²»ČÜÓŚĻõĖį£¬ŌņĻČ¼ÓĻõĖįŅųČÜŅŗÉś³É°×É«³Įµķ£¬ŌŁµĪ¼ÓĻ”ĻõĖįÖĮ³ŹĖįŠŌ£¬ČŌÓŠ°×É«³Įµķ£¬ĖµĆ÷ŌČÜŅŗÖŠÓŠCl-£¬¹ŹEÕżČ·£»
F£®ĻõĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬ČÜŅŗÖŠæÉÄÜŗ¬ÓŠSO32-£¬æÉŃõ»ÆÉś³ÉSO42-£¬¹ŹF“ķĪó£»
G£®ĻČ¼ÓBaCl2ČÜŅŗÉś³É°×É«³Įµķ£¬æÉÄÜÉś³ÉAgCl³Įµķ£¬Ó¦ĻČ¼ÓČėŃĪĖį£¬ŌŁ¼ÓČėĀČ»Æ±µ£¬¹ŹG“ķĪó£»
H£®¼ÓČėŃĪĖįĖį»Æ£¬ÓŠĪŽÉ«ĪŽĪ¶ĘųĢå²śÉś£¬ČÜŅŗÖŠæÉÄÜŗ¬ÓŠHCO3-£¬¹ŹG“ķĪó£®
¹Ź“š°øĪŖ£ŗCE£»
£Ø3£©¢ŁĻņBa£ØHCO3£©2ČÜŅŗÖŠµĪČėNaHSO4ČÜŅŗ£¬ÖĮBa2+øÕŗĆ³ĮµķĶźČ«£¬·“Ӧɜ³ÉBaSO4”¢H2O”¢CO2£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖBa2++SO42-+H++HCO3-=BaSO4++H2O+CO2”ü£¬
¹Ź“š°øĪŖ£ŗBa2++SO42-+H++HCO3-=BaSO4++H2O+CO2”ü£»
¢ŚĻņBa£ØOH£©2ČÜŅŗÖŠµĪČėNaHSO4ČÜŅŗ£¬ÖĮøÕŗĆÖŠŗĶĶźČ«£¬¶žÕß°“ĪļÖŹµÄĮæ±ČÖµ1£ŗ2·“Ó¦£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖBa2++2OH-+2H++SO42-=BaSO4+2H2O£¬
¹Ź“š°øĪŖ£ŗBa2++2OH-+2H++SO42-=BaSO4+2H2O£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°ĪļÖŹµÄ·ÖĄė”¢Ģį“攢Ąė×ӵļģŃéŅŌ¼°Ąė×Ó·½³ĢŹ½µÄŹéŠ“£¬ĪŖøßĘµæ¼µć£¬²ąÖŲĖ«»łµÄ漲飬ӊĄūÓŚÅąŃųѧɜĮ¼ŗƵÄæĘѧĖŲŃų£¬ĢįøßѧĻ°µÄ»ż¼«ŠŌ£¬×¢Ņā°ŃĪÕĪļÖŹµÄŠŌÖŹŅŌ¼°ŹµŃéµÄŃĻĆÜŠŌŗĶæÉŠŠŠŌµÄĘĄ¼Ū£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4 L H2OĖłŗ¬µÄ·Ö×ÓŹżĪŖNA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬1 mol HDŗ¬ÓŠÖŠ×Ó×ÜŹżĪŖ2NA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬32 g O2ÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA | |
| D£® | 100 mL 1 mol•L-1K2SO4ČÜŅŗÖŠŗ¬ÓŠµÄ¼ŲĄė×ÓŹżĪŖ0.1 NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ļ§Ģ¬µŖ·ŹŗĶ²ŻÄ¾»Ņ?ŗ¬K2CO3ÄÜ»ģŗĻŹ©ÓĆ | |
| B£® | »Æ·ŹŗĶÅ©¼Ņ·Ź?ČēĀĢ·Ź?²»æÉ»ģŗĻŹ©ÓĆ | |
| C£® | ”°ŃĪ¼īµŲ”±ÖŠÓŠNa2CO3Ķعż¼ÓŹÆøąŹ¹Ö®Éś³ÉĢ¼ĖįøĘ£¬ÕāŃłøł¾ŻĘ½ŗāŅʶÆŌĄķ£¬Ėę×Åc£ØCO32-£©ÅØ¶ČµÄ½µµĶ£¬”°ŃĪ¼īµŲ”±µÄ¼īŠŌ½µµĶ | |
| D£® | ø“ŗĻ·Ź?ČēĮ×ĖįĒā¶žļ§?ŗĶÉśŹÆ»ŅÄÜŅ»ĘšŹ©ÓĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| »ģŗĻĪļ £ØĄØŗÅÄŚĪŖÉŁĮæŌÓÖŹ£© | ŹŌ¼Į £Ø×ćĮ棩 | ·ÖĄė·½·Ø | |
| A | ±½£Ø±½·Ó£© | ||
| B | ŅŅĖįŅŅõ„£ØŅŅĖį£© | ||
| C | ŅŅ“¼£ØĖ®£© |
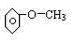 £®
£®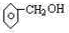 £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ü¢Ż¢Ž¢ß | B£® | ¢Ł¢Ś¢Ü¢Ż¢Ž | C£® | ¢Ś¢Ü¢Ż¢Ž¢ß | D£® | ¢Ś¢Ü¢Ż¢Ž¢ß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
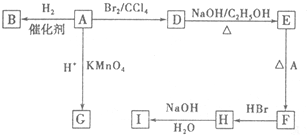
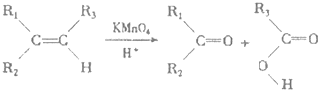
 £®
£®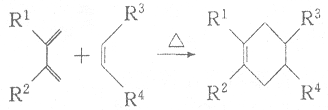
 £®
£®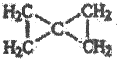 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | c£ØNH4+£©£¾c£ØSO42-£© | B£® | c£ØNH4+£©+c£ØNH3•H2O£©=2c£ØSO42-£© | ||
| C£® | c£ØNH4+£©+c£ØH+£©=c£ØSO42-£©+c£ØOH-£© | D£® | ¼ÓČėÉŁĮæNaOH¹ĢĢ壬c£ØNH4+£©Ōö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
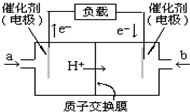 £Ø1£©ėĀ£ØN2H4£©ÓÖ³ĘĮŖ°±£¬ŹĒŅ»ÖÖæÉČ¼ŠŌµÄŅŗĢ壬æÉÓĆ×÷»š¼żČ¼ĮĻ£®·“Ó¦Ź±ŹĶ·Å“óĮæČČ²¢æģĖŁ²śÉś“óĮæĘųĢ壮ŅŃÖŖŌŚ101kPa£¬298KŹ±£¬1molŅŗĢ¬N2H4ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³ÉN2ŗĶĖ®ÕōĘų£¬·Å³öČČĮæ624kJ£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ŹĒN2H4£Øl£©+O2£Øg£©=N2£Øg£©+2H2O£Øg£©”÷H=-624KJ/mol£®ÓÖÖŖ£ŗH2O£Øg £©=H2O £Øl£©”÷H=-44kJ•mol-1£¬Čō1molŅŗĢ¬N2H4ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³ÉN2ŗĶŅŗĢ¬Ė®£¬Ōņ·Å³öČČĮæĪŖ712kJ£®
£Ø1£©ėĀ£ØN2H4£©ÓÖ³ĘĮŖ°±£¬ŹĒŅ»ÖÖæÉČ¼ŠŌµÄŅŗĢ壬æÉÓĆ×÷»š¼żČ¼ĮĻ£®·“Ó¦Ź±ŹĶ·Å“óĮæČČ²¢æģĖŁ²śÉś“óĮæĘųĢ壮ŅŃÖŖŌŚ101kPa£¬298KŹ±£¬1molŅŗĢ¬N2H4ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³ÉN2ŗĶĖ®ÕōĘų£¬·Å³öČČĮæ624kJ£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ŹĒN2H4£Øl£©+O2£Øg£©=N2£Øg£©+2H2O£Øg£©”÷H=-624KJ/mol£®ÓÖÖŖ£ŗH2O£Øg £©=H2O £Øl£©”÷H=-44kJ•mol-1£¬Čō1molŅŗĢ¬N2H4ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³ÉN2ŗĶŅŗĢ¬Ė®£¬Ōņ·Å³öČČĮæĪŖ712kJ£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com