
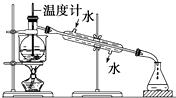
 (1)从含碘的有机溶液中提取碘和回收有机溶剂,需要经过蒸馏,指出下面蒸馏装置图中的错误之处.
(1)从含碘的有机溶液中提取碘和回收有机溶剂,需要经过蒸馏,指出下面蒸馏装置图中的错误之处.分析 (1)蒸馏是利用物质的沸点不同分离相互溶解的沸点不同的液体,蒸馏时用到蒸馏烧瓶、酒精灯、冷凝管、牛角管、锥形瓶等仪器,注意温度计水银球应处在蒸馏烧瓶的支管口附近,冷凝管应从下口进水,上口出水,以保证水充满冷凝管,起到充分冷凝的作用,为防止溶液爆沸,应加入少量碎瓷片,据此解答;
(2)依据水浴加热优点:使蒸馏烧瓶受热均匀,便于控制温度解答;
碘的沸点高于四氯化碳,四氯化碳先被蒸出.
解答 解:(1)①蒸馏实验中,温度计测量的是蒸汽的温度所以,温度计下端的水银球不能插入溶液中,温度计的水银球在蒸馏瓶的支管口下沿处;
②为到达最佳冷凝效果,冷凝水应下进上出;
③烧杯加热应垫上石棉网;
故答案为:①温度计下端的水银球不能插入溶液中;
②冷凝管进出水的方向颠倒;
③加热烧杯未垫上石棉网;
(2)由题意知:有机溶剂为CCl4(沸点为77℃),低于水的沸点,所以选择水浴加热使蒸馏烧瓶受热均匀,便于控制温度;
碘的沸点为184℃,故最后晶态碘在蒸馏烧瓶里聚集;
故答案为:有机溶剂沸点低于100℃,使蒸馏烧瓶受热均匀,便于控制温度;蒸馏烧瓶.
点评 本题考查了蒸馏实验,明确蒸馏实验的原理及仪器实验方法是解题关键,注意温度计位置、冷凝水方向,为高频考题,侧重考查学生对基础实验知识掌握的熟练程度,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含有Br、Fe2+、I-的溶液中欲只氧化I-而不氧化Br、Fe2+,可用FeBr3作试剂 | |
| B. | 向Fel2溶液中通入少量Cl2,反应的离子方程式为:2Fe2++Cl2═2Fe3++2C1- | |
| C. | 向FeBr2溶液中通入足量Cl2,反应的离子方程式为:2Fe2++2Br-+2Cl2═2Fe3++Br2+4CI- | |
| D. | 向FeCl2溶液中滴加足量碘水,能发生反应:2Fe2++12═2Fe3++2I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该物质属于芳香族化合物 | B. | 它的分子式是C16H10N2O2 | ||
| C. | 靛蓝完全燃烧生成二氧化碳和水 | D. | 它是不饱和的有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,最简便的流程需要下列反应的顺序应是( )
,最简便的流程需要下列反应的顺序应是( )| A. | b、d、f、g、h | B. | e、d、c、a、h | C. | a、e、d、c、h | D. | b、a、e、c、f |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Al (OH)3 |
| 开始沉淀时的pH | 7.0 | 1.9 | 3.4 |
| 完全沉淀时的pH | 9.0 | 3.2 | 4.7 |
| 实验操作 | 现象 | 结论 |
| 取适量产品于洁净烧杯中,加入适量蒸馏水,充分搅拌,静置,滤去沉淀. | 得黄棕色溶液 | |
| 取少量溶液于试管中,滴加溶液 ①0.05mol/L酸性高锰酸钾; | ②溶液不褪色; | 溶液中不含Fe2+ |
| 取少量溶液于试管中,滴加0.1 mol/L BaCl2溶液,再滴加20% HNO3溶液 | ③产生白色沉淀; | 溶液中含有SO${\;}_{4}^{2-}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com