
| A、已知2H2(g)+O2(g)=2H2O(g),△H=-483.6kJ?mol-1,则H2的燃烧热为-241.8kJ?mol-1 | ||||||||||
B、已知:25℃时,
| ||||||||||
C、反应Fe(s)+5CO(g)?Fe(CO)5(g)的平衡常数表达式为K=
| ||||||||||
D、0.1mol?L-1的酒石酸(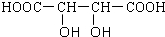 )与0.1mol?L-1的NaOH混合后:c(HC4H4O6-)+2c(C4H4O62-)=c(Na+)+c(H+)-c(OH-) )与0.1mol?L-1的NaOH混合后:c(HC4H4O6-)+2c(C4H4O62-)=c(Na+)+c(H+)-c(OH-) | ||||||||||


科目:高中化学 来源: 题型:
| A、反应开始时的速率:甲>乙 |
| B、反应所需时间:甲<乙 |
| C、反应开始时,酸的物质的量浓度:甲>乙 |
| D、反应结束时,pH:甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol/L氢氰酸溶液的pH约为3 |
| B、常温下,pH=a的HCN稀释100倍后所得溶液pH<(a+2)[(a+2)<7] |
| C、10mL 1mol/L HCN恰好与10mL 1mol/L NaOH溶液完全反应 |
| D、NaCN溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
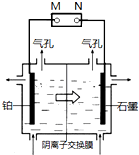 制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向.下列说法不正确的是( )
制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向.下列说法不正确的是( )| A、M是电源的负极 | ||||
| B、左侧气孔逸出的气体可能为副产物H2 | ||||
C、电解槽中发生的总反应为:MnSO4+2H2O
| ||||
| D、若用阳离子交换膜代替阴离子交换膜,阳极可能得到 MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁和盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、氯化铁和铜反应:Fe3++Cu=Fe2++Cu2+ |
| C、澄清石灰水与碳酸钠溶液混合:Ca(OH)2+CO32-=CaCO3↓+2OH- |
| D、用醋酸除水垢:2CH3COOH+CaCO3=2CH3COO-+Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
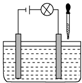 在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液时,则灯光由亮变暗至熄灭后又逐渐变亮的是( )
在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液时,则灯光由亮变暗至熄灭后又逐渐变亮的是( )| A、盐酸中逐滴加入食盐溶液 |
| B、醋酸中逐滴加入氢氧化钠溶液 |
| C、饱和石灰水中不断通入CO2 |
| D、醋酸中逐滴加入氨水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com