
纳米氧化镁具有特殊的热、光、电、力学等性能,下图是利用海水制备纳米氧化镁的流程图。已知:Ksp(MgCO3)=6.8×10-6,Ksp[Mg(OH)2]=1.8×10-11。
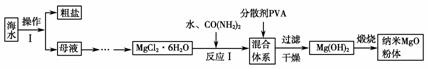
回答下列问题:
(1)操作Ⅰ后在室温下测得母液中镁离子浓度为1.8×10-3 mol·L-1,要使镁离子产生沉淀,溶液的pH最低应为________。
(2)反应Ⅰ中CO(NH2)2与H2O反应生成CO2和NH3·H2O,还发生的另一主要化学反应的离子方程式为____ ___________________________。
___________________________。
(3)某科研小组研究反应Ⅰ在温度为378~398 K时的反应时间、反应物配比等因素对制备纳米氧化镁产率的影响。请完成以下实验设计表(表中不要留空格):
| 实验 编号 | T/K | 反应 时间/h | 反应物的物质的量配比n[CO(NH2)2]∶ n(MgCl2·6H2O) | 实验目的 |
| ① | 378 | 3 | 3∶1 | (1)实验①和③探究________。 (2)实验②和④探究________。 (3)实验②和________探究反应时间对产率的影响。 |
| ② | 378 | 4 | 4∶1 | |
| ③ | 378 | 3 | ||
| ④ | 398 | 4 | 4∶1 |
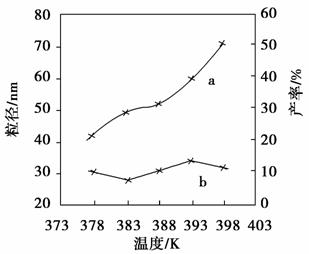
(4)如图为反应Ⅰ的温度对纳米MgO产率(曲线a)和粒径(曲线b)的影响,请你归纳出温度对纳米MgO的制备有何影响(至少写出一条):___________________________________。
解析 本题考查纳米氧化镁的制备, 意在考查考生运用化学反应原理解决问题的能力以及控制变量法在实验中的应用。
意在考查考生运用化学反应原理解决问题的能力以及控制变量法在实验中的应用。
(1)当镁离子开始沉淀时,c(OH-)= mol·L-1=1×10-4 mol·
mol·L-1=1×10-4 mol·
L-1,根据室温下KW=1×10-14可得pH=10。
(2)氯化镁与氨水发生复分解反应:Mg2++2NH3·H2O===Mg(OH)2↓+
2NH4+。(3)本题考查控制变量法的运用。实验①和③的反应温度、反应时间都相同,所以研究的是反应物的物质的量配比对 产率的影响,结合其他实验可知实验③中反应物的物质的量配比为4∶1。实验②和④的反应时间、反应物的物质的量配比都相同,但温度不同,显然是探究温度对产率的影响。探究反应时间对产率的影响,需使反应温度、反应物物质的量配比都相同,显然是②和③。(4)从图像可以看出,在378~398 K,纳米MgO的粒径大小无明显变化;在383 K时有利于形成较小的颗粒;产率随温度的升高而增大等。
产率的影响,结合其他实验可知实验③中反应物的物质的量配比为4∶1。实验②和④的反应时间、反应物的物质的量配比都相同,但温度不同,显然是探究温度对产率的影响。探究反应时间对产率的影响,需使反应温度、反应物物质的量配比都相同,显然是②和③。(4)从图像可以看出,在378~398 K,纳米MgO的粒径大小无明显变化;在383 K时有利于形成较小的颗粒;产率随温度的升高而增大等。
答案 (1)10 (2)Mg2++2NH3·H2O===Mg(OH)2↓+2 NH4+
NH4+
(3)4∶1 反应物的物质的量配比对产率的影响 温度对产率的影响 ③
(4)在378~398 K,纳米MgO的粒径大小无明显变化(或在383 K时有利于形成较小的颗粒;产率随温度的升高而增大等其他合理答案)


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
 |
在体积一定的密闭容器中进行如下反应:X2(g)+2Y2(g) 2 Z(g),已知X2、Y2、Z的起始浓度分别为a mol/L、b mol/L、 0.2mol/L(非平衡态),在一定条件下,当反应达到平衡时,Z的浓度为 0.3mol/L,则下列判断正确的是 ( )
A.b ≤ 0.1mol/L
B.达平衡时,X2的正反应速率与Y2的逆反应速率相等
C.a ≥ 0.05 mol/L
D.该平衡时气体物质的量浓度之和小于(a+ b+0.2)mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
在乙酸、乙醇和浓硫酸混合物中,加入H218O,过一段时间后,18O存在于( )
A.只存在于乙酸分子中 B.存在于乙酸和乙酸乙酯中分子中
C.只存在于乙醇分子中 D.存在于水和乙酸分子中
查看答案和解析>>
科目:高中化学 来源: 题型:
利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如下

(1)装置B的作用:①控制气流速度;②均匀混合气体;③__________________________
(2)写出Cl2与CH4在光照条下反应方程式(任写一个):
(3)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式______________________。
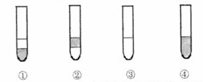
(4)取装置D中试管内液体2mL,加到含有2mL溴水的试管中,然后充分振荡该试管,并静置。下列图示中,可表示试管内液体的正确现象是 (填写编号,图中灰色表示有色液体)。
(5)实验前,E烧杯中有100mL水,实验结束时,E烧杯中溶液的质量分数为0.073.则参加取代反应氯气的体积(标况)为 。(假设取代反应生成的氯化氢气体全部被E烧杯中的水吸收;忽略其他反应产生的氯化氢气体)
(6)该装置存在缺陷,因为没有进行尾气处理,其尾气的主要成分可能是 。(填写化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
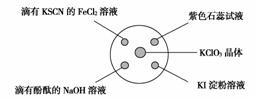
已知:KClO3+6HC l(浓)===KCl+3Cl2↑+3H2O。如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )
l(浓)===KCl+3Cl2↑+3H2O。如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )
| 选项 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液变红色 | Cl2具有还原性 |
| B | 滴有酚酞的NaOH溶液退色 | Cl2具有酸性 |
| C | 石蕊试液先变为红色后退色 | Cl2具有漂白性 |
| D | KI淀粉溶液变蓝色 | Cl2具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合气体中可能有H2、CO、CO2、HCl、NH3及水蒸气中的两种或多种,当混合气体依次通过①适量澄清石灰水(无浑浊现象);②氢氧化钡溶液(有浑浊现象);③浓硫酸(无现象);④灼热的氧化铜(变红);⑤无水硫酸铜(变蓝);则对该混合气体的成分判断正确的是( )。
A.一定没有CO2,肯定有CO和H2
B.一定有CO、CO2和水蒸气
C.一定有H2、HCl和CO2
D.有CO2、NH3和水蒸气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语中,书写或说法正确的是( )
A.乙烯的结构简式:CH2CH2
B.乙醇含有的官能团是—OH,带一个单位负电荷
C.丙烷的球棍模型为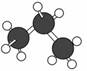
D.乙酸的分子式:C2H4O
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物M共7.4g,与足量的氧气反应后,将所得气体依次通过盛有浓硫酸和碱石灰的装置,两装置分别增重9g和17.6g。同温同压下,M蒸气的密度是H2的37倍,则能够与钠反应放出H2 的M的同分异构体的数目为(不考滤立体异构) ( )
A.8 B.6 C.4 D.2
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C4H8O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯共有 ( )
A. 1种 B. 5种 C. 9种 D.12种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com