
| A. | 漂白粉露置在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 向滴有酚酞的硅酸钠溶液中边加边振荡地滴加盐酸至红色变浅并接近消失:2H++SiO32-═H2SiO3(胶体) | |
| C. | 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O═2SO32-+4Cl-+6H+ | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3═FeO42-+3Cl-+H2O+4H+ |
分析 A.漂白粉的主要成分为次氯酸钙,次氯酸钙与二氧化碳反应生成碳酸钙沉淀;
B.硅酸钠为强碱弱酸盐,其溶液呈碱性,硅酸钠和稀盐酸反应生成难溶性硅酸和氯化钠,氯化钠为强碱强酸盐,其溶液呈中性;
C.氯气具有强氧化性,亚硫酸根离子被氧化成硫酸根离子;
D.强碱性溶液中,反应产物中不会存在氢氧根离子.
解答 解:A.Ca(ClO)2是漂白粉中有效成分,漂白粉置于空气中生成次氯酸和碳酸钙沉淀,正确的离子方程式为:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO,故A错误;
B.硅酸钠为强碱弱酸盐,其溶液呈碱性,硅酸钠和稀盐酸反应生成难溶性硅酸和氯化钠,氯化钠为强碱强酸盐,其溶液呈中性,离子方程式为2H++SiO32-═H2SiO3(胶体),故B正确;
C.氯气具有强氧化性,能够将S2O32-氧化成SO42-,正确的离子方程式应为:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+,故C错误;
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4,反应的离子方程式为:2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O,故D错误;
故选B.
点评 本题考查离子方程式的书写,题目难度中等,注意掌握离子方程式的书写原则,明确弱电解质、难溶物质、气体、氧化物等在离子方程式中写成化学式.


科目:高中化学 来源: 题型:多选题
| A. | 纤维素在稀硫酸、加热的条件下水解 | |
| B. | 棉制品吸湿性好和分子中具有-OH有关 | |
| C. | 纤维指的就是纤维素 | |
| D. | 纤维素因分子结构中含-OH,可和浓HNO3发生硝化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当一个化学反应达到一定反应限度时,该反应就停止了 | |
| B. | 化学反应速率为“0.8mol•L-1•s-1”表示的意思是:时间为1s时,某物质的浓度为0.8mol•L-1 | |
| C. | 根据化学反应速率的大小可以知道化学反应进行的限度 | |
| D. | 对于不同的化学反应而言,化学反应速率大的不一定反应就快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 锌片是正极 | |
| B. | 铜片上发生的反应为 Cu-2e-═Cu2+ | |
| C. | 电子由铜片通过导线流向锌片 | |
| D. | 该装置能够将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
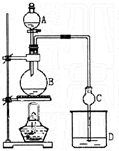 某课外小组设计的实验室制取乙酸乙酯的装置如图所示. 已知①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH;②有关有机物的沸点如下表:
某课外小组设计的实验室制取乙酸乙酯的装置如图所示. 已知①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH;②有关有机物的沸点如下表:| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
 CH3CO18OCH2CH3+H2O.
CH3CO18OCH2CH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同系物:CH2O2、C2H4O2、C3H6O2 | B. | 化合物:五水硫酸铜、烧碱、冰醋酸 | ||
| C. | 电解质:Al2O3、NaOH、CaCO3 | D. | 同素异形体:金刚石、石墨、足球烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,4g CH4含有NA个C-H共价键 | |
| B. | 1 mol Fe与过量的稀硝酸反应过程中转移的电子数为2NA | |
| C. | 常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA | |
| D. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com