
【题目】下列关于乙醇的说法正确的是
A.是无色无味的液体B.能使紫色石蕊试液变红
C.可以作燃料D.不能与金属钠反应
科目:高中化学 来源: 题型:
【题目】为解决能源短缺问题,工业生产中应合理利用化学能。
(1)25℃,1.01×105Pa时,实验测得,4g氢气在O2中完全燃烧生成液态水,放出572kJ的热量,则表示H2的燃烧热的热化学方程式为________________________________。
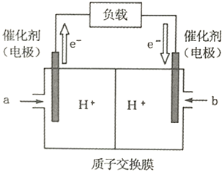
(2)下图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从_________处通入(填“a”或“b”),电池内部H+向_________(填“左”或“右”)移动。写出电池负极的电极反应式_________________________________。
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
化学键 | H-H | N-H | N≡N |
键能/ kJ·mol-1 | 436 | a | 945 |
已知:N2(g)+3H2(g)=2NH3(g) △H=-93 kJ·mol-1。试根据表中所列键能数据计算a的数值__________。
(4)已知:C(s,石墨)+O2(g)=CO2(g) △H1=-393.5 kJ·mol-1 ①
2H2(g)+O2(g)=2H2O(1) △H2=-571.6 kJ·mol-1 ②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(1) △H3=-2599 kJ·mol-1 ③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)=C2H2(g)的△H=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】面对日益加剧的能源危机,我国《能源发展纲要》中倡导大力发展替代能源,如风能、电能等,要大力开发电动自行车、电动摩托车、电动汽车。回答下列问题:
(1)下列物质中可以作为燃料电池的负极反应物的是(____)
A.CH4 B.H2 C.C2H5OH D.CO2
(2)若用CH4作燃料,氢氧化钾溶液作电解质溶液,写出负极上的电极反应式_______________。
(3)电池工作时,溶液中KOH的物质的量浓度________(填“增大”“不变”或“减小”)。
(4)某温度下的饱和Na2SO4溶液的溶解度为25 g,用甲烷燃料电池进行电解,当阳极产生3.36 L(标准状况)气体时,电路中通过电子的物质的量为_______,消耗甲烷的物质的量为_______,此时,析出Na2SO4·10H2O的质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的表示方法多种多样,下面是常用的有机物的表示方法:
①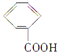 ②
②![]() ③CH4 ④
③CH4 ④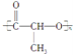 ⑤
⑤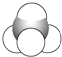
⑥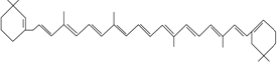 ⑦
⑦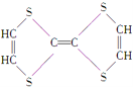
⑧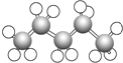 ⑨
⑨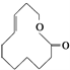 ⑩
⑩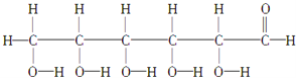
(1)上述表示方法中属于结构简式的为 _________;属于结构式的为 _______________;属于键线式的为 ________________;属于比例模型的为 _______________;属于球棍模型的为 __________________;
(2)写出⑨的分子式: ________________;
(3)②的分子式为 ________________,最简式为 ______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或做法正确的是
A.液氯是混合物,氯水是纯净物
B.金属钠着火燃烧时,用泡沫灭火器灭火
C.铝比铁活泼,所以铝比铁更容易被腐蚀
D.CO2通入可溶性硅酸盐中析出硅酸胶体,所以硅酸的酸性小于碳酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应: 2 A(g) + B(g) ![]() 3 C(g) + D(g)。试根据下图判断正确的是
3 C(g) + D(g)。试根据下图判断正确的是

A. 温度T1℃ 比 T2℃高
B. 正反应为放热反应
C. 甲图纵轴可以表示A的转化率
D. 甲图纵轴可以表示混合气体平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中可用如图制备乙炔,回答下列问题
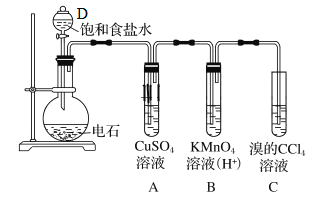
(1)仪器D名称_______________________。
(2)制取乙炔的化学方程式_______________________________________________。
(3)试管A观察到的现象_______________________。
(4)写出C发生的化学方程式______________________________________________。
(5)若没有A装置,观察到B褪色,且有浅黄色浑浊,请写出生成浅黄色浑浊的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫单质及其化合物在工农生产中有着重要的应用,请回答下列问题:
(1)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下:
①CaSO4(s)+CO(g)=CaO(s)+SO2(g)+CO2(g) △H=+210.5kJ·mol-1
②1/4CaSO4(s)+CO(g)=1/4CaS(s)+CO2(g) △H=-47.3kJ·mol-1
反应:CaO(s)+3CO(g)+SO2(g)=CaS(s)+3CO2(g) △H=_____________kJ·mol-1
(2)下图为密闭容器中H2S气体分解生产H2和S2(g)的平衡转化率与温度、压强的关系。
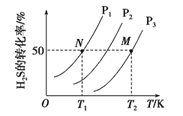
该反应平衡常数的大小关系为K(T1) ____K(T2)(填“>”、“=”或“<”),理由是____。用各物质的平衡分压代替平衡浓度表示反应的平衡常数,记为Kp,计算该反应在T1温度下的Kp=_________(用p1表示)。
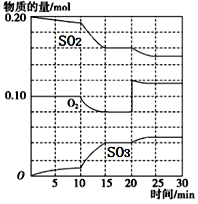
(3)在一定条件下,二氧化硫和氧气发生反应:2SO2(g)+O2(g) ![]() 2SO3 (g)△H<0。据下图判断,反应进行至20min时,曲线发生变化的原因是________________(用文字表达);10min到15min的曲线变化的原因可能是________(填写编号)。
2SO3 (g)△H<0。据下图判断,反应进行至20min时,曲线发生变化的原因是________________(用文字表达);10min到15min的曲线变化的原因可能是________(填写编号)。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加SO2的物质的量
(4)烟气中SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=__________________(用含硫微粒浓度的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种高效消毒剂,可用如下反应制得:2NaClO3+Na2SO3+H2SO4![]() 2ClO2↑+2Na2SO4+H2O,下列说法正确的是( )
2ClO2↑+2Na2SO4+H2O,下列说法正确的是( )
A. 该反应属于复分解反应
B. NaClO3被还原,发生还原反应
C. 反应中Na2SO3作氧化剂
D. 生成6.75 g ClO2时,转移0.2 mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com