
| A. | 常温常压下,11.2L氧气中所含有的原子数为NA | |
| B. | 17g的NH3分子中含有的电子数为10NA | |
| C. | 常温常压下,48g O3含有的氧原子数为3NA | |
| D. | 标准状况下,11.2LH2O中所含有的分子数为0.5NA |
分析 A.根据气体摩尔体积的使用条件判断,标准状况气体摩尔体积为22.4L/mol;
B.物质的量n=$\frac{m}{M}$,1个氨气分子含10个电子;
C.氧原子守恒,计算48g氧原子物质的量得到氧原子数;
D.标准状况水不是气体.
解答 解:A.常温常压下,气体摩尔体积小于22.4L/mol,所以11.2L氧气物质的量小于0.5mol,故A错误;
B.17g的NH3分子物质的量=$\frac{17g}{17g/mol}$=1mol,1mol氨气分子中含有的电子数为10NA,故B正确;
C.常温常压下,48g O3含有的氧原子数=$\frac{48g}{16g/mol}$×NA=3NA,故C正确;
D.标准状况下,水不是气体,气体摩尔体积大于22,4L/mol,11.2LH2O中所含有的分子数小于0.5NA,故D错误;
故选BC.
点评 本题考查了阿伏伽德罗常数的应用,主要是物质的量和微粒数的计算关系分析、气体摩尔体积的应用条件等知识,掌握基础是解题关键,题目难度不大.


 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:选择题
| A. | 硫酸遇明火发热爆炸 | |
| B. | 浓硫酸遇水发热爆炸 | |
| C. | 铁与水反应产生氢气,氢气接触空气后遇明火爆炸 | |
| D. | 稀释后的硫酸与铁反应产生氢气接触明火爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
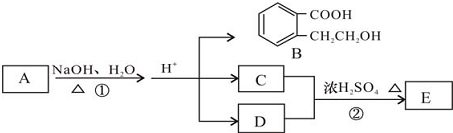
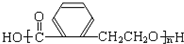 .
.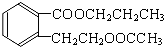 +2 NaOH$\stackrel{△}{→}$
+2 NaOH$\stackrel{△}{→}$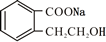 +CH3COONa+CH3CH2CH2OH.
+CH3COONa+CH3CH2CH2OH.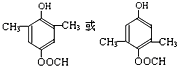 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

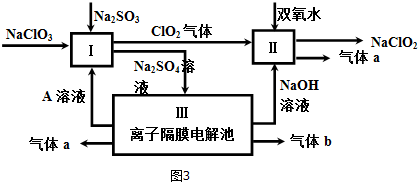
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
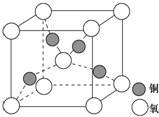 目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
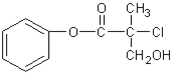
| A. | 1mol A最多能与4mol H2发生加成反应 | |
| B. | 有机物A可以在一定条件下与HBr发生反应 | |
| C. | 有机物A与浓硫酸混合加热,可以发生消去反应 | |
| D. | 1mol A与足量的NaOH溶液反应,最多可以消耗2mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
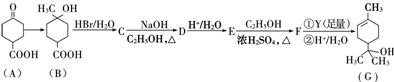
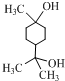
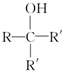 ,请回答下列问题:
,请回答下列问题: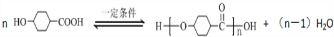 .
. .
.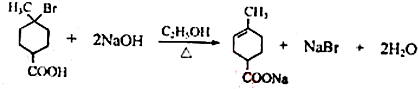 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com