
| A.反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 | ||
| B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | ||
C.CH3COOH溶液加水稀释后,溶液中
| ||
| D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
| c(CH3COOH) |
| c(CH3COO-) |


科目:高中化学 来源:不详 题型:单选题
| A.熵增加且放热的反应一定是自发反应 |
| B.自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应 |
| C.凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应 |
| D.非自发反应在任何条件下都不能发生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
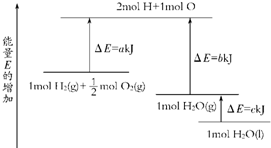
A.H2(g)+
| ||
| B.2H2(g)+O2(g)═2H2O(g)△H=2(b-a)kJ?mol-1 | ||
C.H2(g)+
| ||
| D.2H2(g)+O2(g)═2H2O(l)△H=2(a-b-c)kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.凡是放热反应都是自发的,由于吸热反应都是非自发的 |
| B.自发反应在恰当条件下才能实现 |
| C.自发反应在任何条件下都能实现 |
| D.自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应的△S<0 |
| B.该反应在任何温度下均能自发进行 |
| C.向容器中充入少量He,平衡向正反应方向移动 |
| D.升高温度平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.C0(g)+2H2(g)=CH30H(1) |
| B.CaCO3(s)+2HCl(aq)=CaCl2(aq)+C02(g)+H20(1) |
| C.(NH4)2C03(s)=C02(g)+2NH3(g)+H20(1) |
| D.CaO(s)+C02(g)=CaC03(s) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g);ΔH<0,则该反应一定能自发进行 |
| B.提取海带中碘元素时,为将I-完全氧化为I2,用HNO3作氧化剂比用H2O2效果好 |
| C.原电池放电过程中,负极质量一定减轻,正极的质量一定增加 |
| D.由于Ksp(MgCO3)<Ksp[Mg(OH)2],因此水垢中MgCO3会逐渐转化为Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 A(g)+2B(g),已知ΔH<0,下列判断正确的是
A(g)+2B(g),已知ΔH<0,下列判断正确的是| A.仅常温下反应可以自发进行 | B.仅高温下反应可以自发进行 |
| C.任何温度下反应均可以自发进行 | D.任何温度下反应均难以自发进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com