
| A. | Na2CO3 | B. | CH3OH | C. | Al2O3 | D. | Cu(OH)2 |
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:解答题
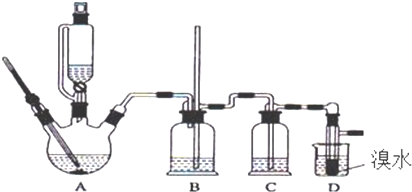
| 乙醇 | 1,2-二溴乙烷 | 醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煮沸饱和FeCl3溶液可以制得Fe(OH)3胶体 | |
| B. | 胶体的本质特征是胶粒半径在1~100nm | |
| C. | 丁达尔现象可以用来区别胶体和溶液 | |
| D. | 溶液能通过滤纸孔隙而胶体的分散质不能通过 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓盐酸与二氧化锰共热 | B. | 浓硫酸与铜共热 | ||
| C. | 过氧化钠与水反应 | D. | 石灰石与稀盐酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内气体的总质量不随时间而变化 | |
| B. | 单位时间内有nmolA2生成的同时就有nmolB2生成 | |
| C. | 2 v(A2)正=v(AB)逆 | |
| D. | A2、B2(g)、AB(g)的浓度之比为1:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
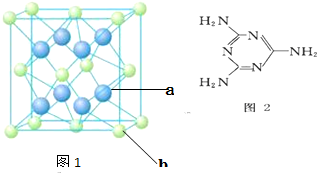 X、Y、Z、M、N、Q P为元素周期表前四周期的7种元素.其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大.P元素的第三电子层处于全充满状态,第四电子层只有一个电子请回答下列问题:
X、Y、Z、M、N、Q P为元素周期表前四周期的7种元素.其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大.P元素的第三电子层处于全充满状态,第四电子层只有一个电子请回答下列问题: ,P元素属于ds区元素.
,P元素属于ds区元素.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com