

���� ��3��Fe��������Ӧ�����Ȼ������壬��Ϊ���ȷ�Ӧ����KSCN��Һ�������ӽ����ҺΪѪ��ɫ��
��4��NaOH�����չ�������������ֹ��Ⱦ������
��5��̽�����������Ƿ����Ȼ�����������������Ӿ��л�ԭ�ԣ���ʹ���������ɫ��ƣ�
��� �⣺��3��Fe��������Ӧ�����Ȼ������壬��Ϊ���ȷ�Ӧ����KSCN��Һ�������ӽ����ҺΪѪ��ɫ����۲쵽������Ϊ��˿����ȼ�ա����ֺ��ȣ������غ�ɫ���̣�ʢ���軯����Һ���Թ����Ժ�ɫ��
�ʴ�Ϊ����˿����ȼ�ա����ֺ��ȣ������غ�ɫ���̣�ʢ���軯����Һ���Թ����Ժ�ɫ��
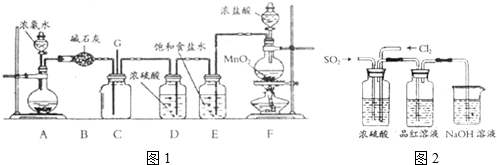
��4���������ж��������ŷ��ڻ����У�������������Һ������������β��Cl2��
�ʴ�Ϊ������β��Cl2��
��5��̽�����������Ƿ����Ȼ�������ʵ�鲽��Ϊ����1����ȡ����ʵ���IJ������еĹ�������������С�ձ��м���������ˮ�����衢�ܽ⣻��2�����μ��������Ը��������Һ���������Һ����ɫ��ȥ����֤��ԭ�������к����Ȼ�����������ԭ�������в����Ȼ�������
�ʴ�Ϊ���μ��������Ը��������Һ���������Һ����ɫ��ȥ����֤��ԭ�������к����Ȼ�����������ԭ�������в����Ȼ�������
���� ���⿼�����ʵ�����ʵ�飬Ϊ��Ƶ���㣬����ʵ��ԭ����ʵ��װ�õ����á����ʵ����ʡ�ʵ�鼼��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע������ʵ�����ƣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
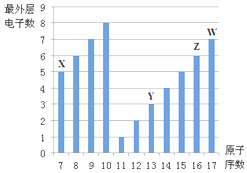 ��ͼ�Dz��ֶ�����Ԫ��������������ԭ�������Ĺ�ϵͼ��
��ͼ�Dz��ֶ�����Ԫ��������������ԭ�������Ĺ�ϵͼ��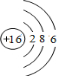 ��
��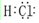 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ�� | N��N | H-O | N-H | O=O |
| E/��kJ/mol�� | 946 | 463 | 391 | 496 |
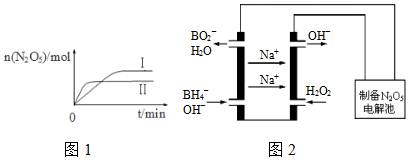
| .01mol/L ����Һ | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol•L-1 NH3•H2O��pHС��13 | |
| B�� | 0.1 mol•L-1 NH4Cl��pHС��7 | |
| C�� | ��ͬ�����£�Ũ�Ⱦ�Ϊ0.1 mol•L-1 NaOH��Һ�Ͱ�ˮ����ˮ�ĵ��������� | |
| D�� | 0.1 mol•L-1 NH3•H2O��ʹ��ɫ��̪��Һ���ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1L0.1mol•L-1NaClO��Һ�У�ClO-����ĿΪ0.1NA | |
| B�� | ���³�ѹ�£�11.2LCH4���еĹ��õ��Ӷ���ĿΪ2NA | |
| C�� | 16gO2��O3��������У���ԭ�ӵ���ĿΪ1.5NA | |
| D�� | 1molFe������Cl2��ȫ��Ӧ��ת�Ƶĵ�����ĿΪ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| t/min | 0 | 1 | 2 | 3 | 4 |
| n��H20��/mol | 0.60 | 0.50 | 0.44 | 0.40 | 0.40 |
| n��CO��/mol | 0.40 | 0.30 | 0.24 | 0.20 | 0.20 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܷ���������Ӧ���뵥���Ʋ��������ͬ���칹����3�� | |
| B�� | ��ˮ���X��4��ͬ���칹�壬����NaHCO3��Ӧ��X��3��ͬ���칹�� | |
| C�� | X��ij��ͬ���칹��ˮ����һ�ֲ������ͨ���������������õ���һˮ����� | |
| D�� | X�����в����ܺ��������ǻ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com