
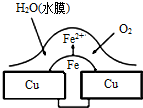
| A、此过程中铜被腐蚀 | B、此过程中电子从Cu移向Fe | C、正极电极反应式为O2+2H2O+4e-═4OH- | D、铁钉表面发生的反应为Fe-3e-═Fe3+ |


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
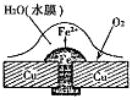 铜板上铁铆钉处的腐蚀原理如图所示,下列有关说法错误的是( )
铜板上铁铆钉处的腐蚀原理如图所示,下列有关说法错误的是( )| A、正极电极反应式为:2H++2e-=H2↑ | B、此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3 | C、此过程中铁先被腐蚀 | D、此过程中电子由铜板向铁 |
查看答案和解析>>
科目:高中化学 来源:吉林省东北师大附中2009届高三第四次摸底考试(化学) 题型:013
|
铜板上铁铆钉处的腐蚀原理如图所示,下列有关说法中,错误的是
| |
| [ ] | |
A. |
正极电极反应式为:O2+2H2O+4e-=4OH- |
B. |
此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
C. |
此过程中铁先被腐蚀 |
D. |
此过程中电子由铜板流向铁 |
查看答案和解析>>
科目:高中化学 来源:2015届福建省宁德市高二上学期质量检测化学试卷A(解析版) 题型:选择题
铜板上铁铆钉处的腐蚀原理如图所示,下列有关说法中正确的是
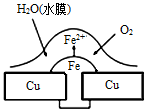
A.此过程中铜被腐蚀
B.此过程中电子从Cu移向Fe
C.正极电极反应式为O2+2H2O+4e-=4OH-
D.铁钉表面发生的反应为Fe-3e- ═ Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:

A.正极电极反应式为2H++2e-![]() H2↑
H2↑
B.此过程中还涉及反应:4Fe(OH)2+2H2O+O2![]() 4Fe(OH)3
4Fe(OH)3
C.此过程中铁先被腐蚀
D.此过程中电子由铜流向铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com