
【题目】下列关于化石燃料的说法正确的是( )
A. 煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气
B. 石油分馏是化学变化,可得到汽油、煤油
C. 石油裂化主要得到乙烯
D. 煤制水煤气是物理变化,是高效、清洁地利用煤的重要途径
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】正丁醚常用作有机反应的溶剂。实验室制备正丁醚的反应和主要实验装置如下:
2CH3CH2CH2CH2OH![]() (CH3CH2CH2CH2)2O + H2O。反应物和产物的相关数据如下
(CH3CH2CH2CH2)2O + H2O。反应物和产物的相关数据如下

相对分子质量 | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
合成反应:
①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。
分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70 mL水的分液漏斗中,振荡后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3 g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11 g。
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为 。
(2)加热A前,需先从 (填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去 ,振荡后静置,粗产物应从分液漏斗的 (填“上”或“下”)口分离出。
(4)步骤④中最后一次水洗的目的为 。
(5)步骤⑤中,加热蒸馏时应收集 (填选项字母)左右的馏分。
a.100℃ b. 117℃ c. 135℃ d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为 ,下层液体的主要成分为 。
(7)本实验中,正丁醚的产率为 。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验事实与相应结论不正确的是
选项 | 实验事实 | 结论 |
A | 其他条件不变,0.01 mol·L-1的酸性KMnO4溶液分别与0.1 mol·L-1的H2C2O4溶液和0.2 mol·L-1的H2C2O4溶液反应,后者褪色时间短 | 当其他条件不变时,增大反应物浓度可以使化学反应速率加快 |
B | 其他条件不变,分别将等体积、等物质的量浓度的Na2S2O3溶液和H2SO4混合液放在冷水和热水中,放在热水中的混合液先出现浑浊 | 当其他条件不变时,反应体系的温度越高,化学反应速率越快 |
C | 将少量MnO2粉末加入盛有10%双氧水的锥形瓶内,在化学反应前后,MnO2的质量和化学性质都没有发生改变 | 催化剂虽然可以加快化学反应的速率,但一定不参与化学反应过程 |
D | 一定条件下,分别在容积为1 L和容积为2 L的两个密闭容器中加入等量的氢气和碘蒸气,发生如下反应:H2(g)+I2(g) | 当其他条件不变时,气态反应体系的压强越大,化学反应速率越快 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟及氟产品在工农业生产中应用非常广泛,回答下列问题:
(1)基态氟原子核外电子的运动状态有__种,这些电子的电子云形状有__种;氟原子的外围电子排布式为______.
(2)NaHF2(氟化氢钠)电解可制氟气,NaHF2中所含作用力的类型有_____;与HF2-互为等电子体的分子有___(举一例).
(3)N2F2(二氟氮烯)分子中,氮原子的杂化轨道类型为____.
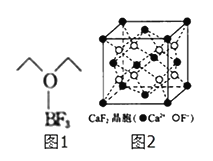
(4)三氟化硼乙醚(如图1)的熔点为-58℃,沸点为126~129℃,它属于__晶体.
(5)氟化钙的晶胞结构如图2所示,晶胞参数α=0.555nm.
①Ca2+、F-的配位数分别为__和__.
②列式表示氟化钙晶体的密度:_________gcm-3(不必计算出结果).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组学生设计了制取KClO3和氯水的实验(装置如下图所示),并进行相关性质的探究。

请按要求回答下列问题:
(1)请在D处方框内画出所需装置,并标注试剂名称__________________。
装置A中发生反应的离子方程式:__________________;当产生2.24mL(标准状况)Cl2时,转移电子数目为_____________________。
(2) B中反应的离子方程式:_________________。该小组学生深入研讨后将B和C装置对调了位置,这样做的优点是__________________。
(3)制取实验结束后,取出上图B中试管,经__________、过滤、洗涤、干燥,得晶体样品。
另取上图C中氯水样品,进行如下实验,请分析:
①在少量样品中滴入几滴石蕊溶液后的现象是________________。
②测定其中所含氯元素的总量;在一定量试样中加入足量的H2O2溶液,充分反应后加热除去过量的H2O2,冷却,在加入足量的硝酸银溶液,经系列操作后,称取沉淀质量。其中加入的H2O2溶液的作用是_______。
(4)欲证明相同条件下HClO的电离常数大于HCO3-,实验方案是____________。
(5)在不同条件下KClO3可将KI氧化成I2或KIO3。该小组设计了系列实验研究反应条件对产物的影响,其中某系列实验数据记录如下表(均室温下进行);
实验 编号 | 试剂及其用量 | |||
0.2mol·L-1kJ/mL | KClO3(s)/g | 6.0mol·L-1H2SO4/mL | H2O/mL | |
1 | 1.0 | 0.1 | 0 | a |
2 | 1.0 | 0.1 | 3.0 | b |
3 | 1.0 | 0.1 | 6.0 | c |
4 | 1.0 | 0.1 | 9.0 | 0 |
①此系列实验中a=____________。此系列实验目的是_________________。
②为使实验现象更加明显,此系列实验中还需添加的一种试剂是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
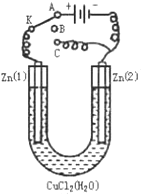
(1)如果把开关K接A,该装置应是 ,Zn(2)极是 极,电极反应式为 。
(2)上述反应进行5min后,置换开关K到C,则该装置是 ,Zn(2)极是 极,电极反应式是 。
(3)上述装置进行2min后,再置换开关K至B,则Zn(1)极发生的化学反应方程式为 ,Zn(2)极发生的有关电化学的反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨的反应如下:N2 + 3H2 ![]() 2NH3。
2NH3。
某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0~50s内的平均反应速率 v(N2) = ______________。
(2)250s时,H2的转化率为________________。
(3)已知![]() 的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中的热量变化_____ kJ。下图能正确表示该反应中能量变化的是_____。
的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中的热量变化_____ kJ。下图能正确表示该反应中能量变化的是_____。

(4)为加快反应速率,可以采取的措施________________。
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离NH3
(5)下列叙述中能说明上述反应达到平衡状态的是_________________。
A.反应中N2与NH3的物质的量之比为1∶2
B.混合气体的总物质的量不随时间的变化而变化
C.单位时间内每消耗a mol N2,同时生成2a mol NH3
D.N2的质量分数在混合气体中保持不变
E.混合气体的平均相对分子质量保持不变
F.混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
A. 充电过程是化学能转化为电能的过程 B. 充电时阳极反应:Ni(OH)2-e-+OH-=NiO(OH)+H2O
C. 放电时负极附近溶液的碱性不变 D. 放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com