
 Si(s)+4HCl(g);ΔH =" +Q" kJ·mol-1(Q>0),下列叙述正确的是
Si(s)+4HCl(g);ΔH =" +Q" kJ·mol-1(Q>0),下列叙述正确的是 | A.反应过程中,若增大压强,能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ |
| C.若单位时间内生成x molHCl的同时,生成x molH2,则反应达到平衡状态 |
| D.使用过量的H2或升高温度都可以提高SiCl4的转化率 |
科目:高中化学 来源:不详 题型:单选题

| A.正反应为放热反应 |
| B.断键吸收的总能量大于成键放出的总能量 |
| C.反应物总能量高于生成物总能量 |
| D.升高温度可增大正反应速率,降低逆反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
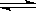 2NH3 △H<0。有甲、乙两个完全相同的容器,向甲容器中加入1molN2和3 molH2,在一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2 molNH3,达平衡时,吸收的热量为Q2。已知Q2=3Q1,则甲容器中,H2的转化率为
2NH3 △H<0。有甲、乙两个完全相同的容器,向甲容器中加入1molN2和3 molH2,在一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2 molNH3,达平衡时,吸收的热量为Q2。已知Q2=3Q1,则甲容器中,H2的转化率为| A.10% | B.20% | C.25% | D.40% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A. 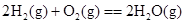 |
| B.C(石墨)+O2(g)===CO2(g) C(金刚石)+O2(g)===CO2(g) (石墨比金刚石稳定) |
C.  |
D. 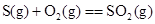 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2CO(g);
2CO(g); 2CO2(g)
2CO2(g)| A.12gC所具有的能量一定高于28gCO所具有的能量 |
| B.56gCO和32gO2所具有的总能量一定高于88gCO2所具有的总能量 |
| C.12gC和32gO2所具有的总能量一定高于44gCO2所具有的总能量 |
| D.将相同质量的碳燃烧,生成CO2比生成CO放出的热量多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝和盐酸反应 | B.灼热的木炭与CO2反应 |
| C.氢气还原氧化铜 | D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.降低温度,可提高b路线中乙醇的转化率 |
| B.从能量消耗的角度来看,b路线制氢更加有利 |
| C.乙醇可通过淀粉等生物原料发酵制得,属于可再生资源 |
| D.由a、b知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ·mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com