
【题目】如下图所示的装置,![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 都是惰性电极。将电源接通后,向乙中滴入酚酞溶液,在
都是惰性电极。将电源接通后,向乙中滴入酚酞溶液,在![]() 极附近显红色。试完成以下问题:
极附近显红色。试完成以下问题:
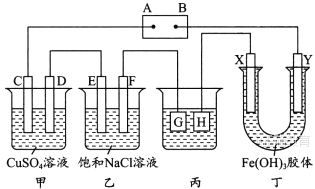
(1)电源![]() 极的名称是________。
极的名称是________。
(2)甲装置中电解反应的总化学方程式是____________。
(3)如果收集乙装置中产生的气体,两种气体的体积比是________。
(4)欲用丙装置给铜镀银,![]() 应该是________(填“铜”或“银”),电镀液的主要成分是________(填化学式) 。
应该是________(填“铜”或“银”),电镀液的主要成分是________(填化学式) 。
(5)装置丁中的现象是________,说明________。
【答案】 正极 ![]()
![]()
![]() 1:1 银 AgNO3 Y极附近红褐色变深 氢氧化铁胶粒带正电荷
1:1 银 AgNO3 Y极附近红褐色变深 氢氧化铁胶粒带正电荷
【解析】(1)装置乙中是饱和NaCl溶液,通电后,在阳极周围溶液中的Cl-比OH-容易放电,则析出氯气,而在阴极周围溶液中H+比Na+容易放电,则析出氢气,使阴极周围溶液中OH-浓度增大而呈碱性,遇酚酞显红色,根据题目叙述在F极附近显红色,则F极为阴极,所以电源B极为负极,A极为正极;
(2)装置甲中是CuSO4溶液,溶液中的Cu2+比H+更容易在阴极放电而析出铜,溶液中的OH-比SO42-容易放电而析出氧气,所以电解反应的总化学方程式为2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4;
2Cu+O2↑+2H2SO4;
(3)装置乙中是饱和NaCl溶液,电解时在阳极析出氯气,在阴极析出氢气,根据电子转移守恒可得,这两种气体的体积约为1:1;
(4)若用丙装置给铜上镀银,因G电极为阳极,所以G为金属银;电镀液的主要成分是AgNO3;
(5)装置丁中进行的是Fe(OH)3胶体的电泳实验,X极为阳极,Y极为阴极,通电后的现象是Y极附近红褐色变深,说明Fe(OH)3胶体微粒带正电荷,通电时移向电解池的阴极。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
Ⅰ.[查阅资料]
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水。其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得产品中常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
(4)硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2=S4O62-+2I-
Ⅱ.[制备产品]实验装置如图所示(省略夹持装置)

实验步骤:
(1)按如图所示组装好装置后,应先_______________(填操作名称),再按图示加入试剂。仪器B和D的作用是____________________________;E中的试剂是__________(选填下列字母编号)。
A.稀H2SO4 B.NaOH溶液 C.饱和NaHSO3溶液
(2)先向烧瓶C中加入Na2S和Na2CO3混合溶液,再向烧瓶A中滴加浓H2SO4。C中反应生成Na2S2O3和CO2,化学方程式为______________________。
(3)待Na2S和Na2CO3完全消耗后,结束反应。过滤C中混合液,滤液经蒸发、结晶、过滤、洗涤、干燥、得到产品。
Ⅲ.[探究与反思]
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择):
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,____________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(2)用I2的标准溶液测定产品的纯度
取10.0g产品,配制成100mL溶液,配制溶液的蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除__________及二氧化碳。取10.00mL溶液。以________溶液为指示剂,用浓度为0.10mol/LI2的标准溶波进行滴定,相关数据记录如下表所示。
编号 | 1 | 2 | 3 |
溶液的体积/mL | 10.00 | 10.00 | 10.00 |
消耗I2标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |
滴定时,达到滴定终点的现象是___________________________________________。Na2S2O3·5H2O在产品中的质量分数是_______________(用百分数表示,且保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是细胞中几种重要化合物的元素组成。下列相关叙述错误的是( )

A. 人体缺乏I元素,将会使甲状腺激素分泌增加
B. 组成生物的蛋白质若含S等元素,这些元素一定位于R基团中
C. 组成核糖和脱氧核糖的元素只有C、H、O
D. 植物发育过程中,如果缺乏了Mg元素,植物的叶片呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不符合ⅦA族元素性质特征的是( )
A.从上到下原子半径逐渐减小
B.易形成﹣1价离子
C.最高价氧化物的水化物显酸性
D.从上到下氢化物的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知pC=-lgc;Ksp[Cu(OH)2]=2.2×10-20和Ksp[Mg(OH)2]=1.8×10-11,测得两种金属离子的PC与pH的变化关系如下图所示。下列说法正确的是

A. 加入氨水调节pH可除去MgS04溶液中的CuSO4杂质
B. pH调到Q点则Mg2+和Cu2+都已沉淀完全
C. 在浓度均为1mo/LCuSO4和MgS04的混合溶液中,存在c(Cu2+)+c(Mg2+)>c(S042-)
D. L1代表pC(Cu2+)随pH变化,L2代表pC(Mg2+)随pH变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科,下列操作或发生事故时的处理方法正确的是
A. 可用燃着的酒精灯引燃另一只酒精灯。
B. 给试管里的液体加热时,试管应与桌面垂直。
C. 配置一定浓度的NaCl溶液时,定容振荡摇匀后,发现液面低于刻度线,再加水到刻度线。
D. 浓硫酸不慎沾在皮肤上,应立即用大量水冲洗,最后涂上3%-5%的小苏打溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中橙红色的![]() 与黄色的
与黄色的![]() 有下列平衡关系:
有下列平衡关系:![]()
![]()
![]() ,把重铬酸钾(
,把重铬酸钾(![]() )溶于水配成稀溶液是橙色的。
)溶于水配成稀溶液是橙色的。
(1)向上述溶液中加入![]() 溶液,溶液呈__________色,因为_________。
溶液,溶液呈__________色,因为_________。
(2)向已加入![]() 溶液的1中再加入过量稀硫酸,则溶液呈__________色,因为__________。
溶液的1中再加入过量稀硫酸,则溶液呈__________色,因为__________。
(3)向原溶液中加入![]() 溶液(已知
溶液(已知![]() 为黄色沉淀)则平衡________,溶液颜色将________。
为黄色沉淀)则平衡________,溶液颜色将________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知25℃时,Ksp(AgCl) =1.8×10-10,Ksp(AgBr) =5.4×10-13,Ksp(AgI) =8.5×10-17。某溶液中含有C1-、Br-和I-,浓度均为0.010mo1·L-1,向该溶液中逐滴加入0.010mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
A. C1-、Br-、I- B. Br-、C1-、I-
C. I-、Br-、C1- D. Br-、I-、C1-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘化钾(即碘离子)的形式存在。实验室里从海藻中提取碘的流程如下图,已知 (Cl2+2KI=2KCl+I2)
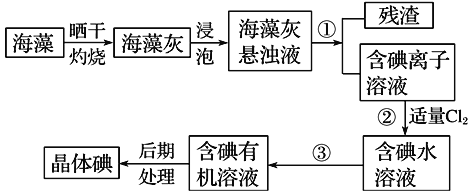
(1)实验室焙烧海带,需要下列仪器中的________(填字母)。
a.试管 b.烧杯c.坩埚 d.泥三角 e.三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①________,③__________。
(3)提取碘的过程中,可选择的有机试剂是________。
A.苯、酒精 B.四氯化碳、苯 C.汽油、醋酸 D.汽油、酒精
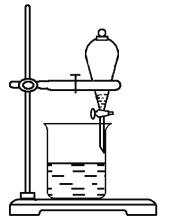
(4)某小组用CCl4萃取碘水中的碘,在如图的分液漏斗中,下层液体呈______色;他们打开分液漏斗活塞,却未见液体流下,原因可能是___________________ 。
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
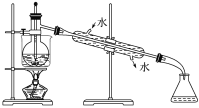
①________________________________________________;
②______________________________________________________;
③________________________________________________________。
(6)进行上述蒸馏操作时,使用水浴加热的目的_______________________,最后晶态碘在________里聚集。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com