
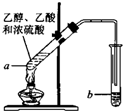
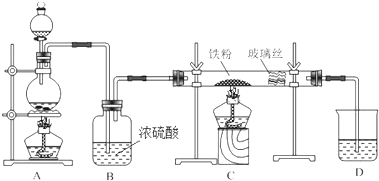
 £Ø1£©ŌŚŹµŃéŹŅæÉŹ¹ÓĆČēĶ¼×°ÖĆÖĘČ”ŅŅĖįŅŅõ„£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŌŚŹµŃéŹŅæÉŹ¹ÓĆČēĶ¼×°ÖĆÖĘČ”ŅŅĖįŅŅõ„£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ·ÖĪö £Ø1£©õ„»Æ·“Ó¦µÄ±¾ÖŹĪŖĖįĶŃōĒ»ł£¬“¼ĶŃĒā£¬øĆ·“Ӧɜ³ÉŅŅĖįŅŅõ„ŗĶĖ®£¬ŹōÓŚČ”“ś·“Ó¦ĒŅĪŖæÉÄę·“Ó¦£¬Éś³ÉµÄõ„ÓƱ§ŗĶĢ¼ĖįÄĘĄ“ĪüŹÕ£»
£Ø2£©AŹĒŅ»ÖÖÖ²ĪļÉś³¤µ÷½Ś¼Į£¬AĪŖŅŅĻ©£¬ÓėäåĖ®·¢Éś¼Ó³É·“Ó¦Ź¹äåĖ®ĶŹÉ«£¬¾Ż“Ė»Ų“š£®
½ā“š ½ā£ŗ£Ø1£©ŹµŃéÖŠÓĆŅŅ“¼ÓėŅŅĖį×÷ÓĆ·¢Éśõ„»Æ·“Ó¦£¬õ„»Æ·“Ó¦µÄ±¾ÖŹĪŖĖįĶŃōĒ»ł£¬“¼ĶŃĒā£¬ŅŅĖįÓėŅŅ“¼ŌŚÅØĮņĖį×÷ÓĆĻĀ¼ÓČČ·¢Éśõ„»Æ·“Ӧɜ³ÉŅŅĖįŅŅõ„ŗĶĖ®£¬øĆ·“Ó¦ĪŖæÉÄę·“Ó¦£¬»Æѧ·½³ĢŹ½ĪŖ£ŗCH3COOH+CH3CH2OH$?_{”÷}^{ÅØĮņĖį}$CH3COOCH2CH3+H2O£¬ŹōÓŚČ”“ś·“Ó¦ĒŅĪŖæÉÄę·“Ó¦£¬Éś³ÉµÄõ„ÓƱ§ŗĶĢ¼ĖįÄĘĄ“ĪüŹÕ£»
¹Ź“š°øĪŖ£ŗCH3COOH+CH3CH2OH$?_{”÷}^{ÅØĮņĖį}$CH3COOCH2CH3+H2O£»Č”“ś·“Ó¦£Ø»ņõ„»Æ·“Ó¦£©£»±„ŗĶĢ¼ĖįÄĘČÜŅŗ£»
£Ø2£©AŹĒŅ»ÖÖÖ²ĪļÉś³¤µ÷½Ś¼Į£¬AĪŖŅŅĻ©£¬·Ö×ÓŹ½ĪŖC2H4£¬AµÄ½į¹¹¼ņŹ½ŹĒCH2=CH2£¬ÓėäåĖ®·¢Éś¼Ó³É·“Ó¦Ź¹äåĖ®ĶŹÉ«£¬
øĆ·“Ó¦ĪŖCH2=CH2+Br2”śCH2BrCH2Br£¬
¹Ź“š°øĪŖ£ŗCH2=CH2£»CH2=CH2+Br2”śCH2BrCH2Br£»¼Ó³É·“Ó¦£®
µćĘĄ ±¾Ģāæ¼²éŅŅĖįŅŅõ„µÄÖʱø£¬½ā“šŹ±Šė×¢Ņāõ„»Æ·“Ó¦µÄŌĄķŗĶ±„ŗĶĢ¼ĖįÄĘČÜŅŗµÄ×÷ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®


 øßÖŠ±ŲĖ¢ĢāĻµĮŠ“š°ø
øßÖŠ±ŲĖ¢ĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗģÄ«Ė®¼Óµ½ĒåĖ®Ź¹Õū±Ė®±äŗģ | B£® | ±łŌŚŹŅĪĀĻĀČŚ»Æ³ÉĖ® | ||
| C£® | Ė®µē½āÉś³ÉĒāĘųŗĶŃõĘų | D£® | ĢśĘ÷ŌŚ³±ŹŖµÄæÕĘųÖŠÉśŠā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŹµŃéŹŅÖĘČ”ŅŅĖįŅŅõ„µÄÖ÷ŅŖ²½ÖčČēĻĀ
ŹµŃéŹŅÖĘČ”ŅŅĖįŅŅõ„µÄÖ÷ŅŖ²½ÖčČēĻĀ| ĪļÖŹ | ŅŅ“¼ | ŅŅĖį | ŅŅĖįŅŅõ„ | ÅØĮņĖį |
| ČŪ£Ø”ę£© | -117.0 | 16.6 | -83.6 | ------ |
| ·Š£Ø”ę£© | 78.0 | 117.9 | 77.5 | 338.0 |
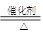 CH3COOC2H5+H2O£®
CH3COOC2H5+H2O£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
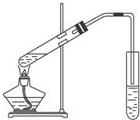 £ØA£©ČēĶ¼ĪŖŹµŃéŹŅÓĆCH3COOHÓėCH3CH218OHÖʱøŅŅĖįŅŅõ„µÄ×°ÖĆ£®
£ØA£©ČēĶ¼ĪŖŹµŃéŹŅÓĆCH3COOHÓėCH3CH218OHÖʱøŅŅĖįŅŅõ„µÄ×°ÖĆ£®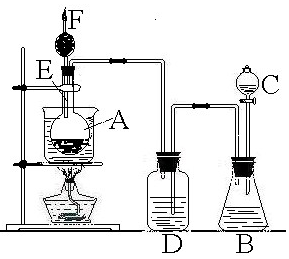
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
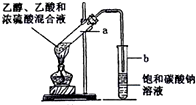 ČēĶ¼ĪŖŹµŃéŹŅÖĘČ”ŅŅĖįŅŅõ„µÄ×°ÖĆ£®
ČēĶ¼ĪŖŹµŃéŹŅÖĘČ”ŅŅĖįŅŅõ„µÄ×°ÖĆ£®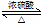 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
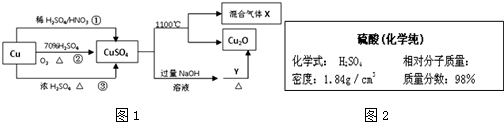
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com