
【题目】已知反应X(g)+Y(g)=Z(g)+W(g)的能量变化如图所示,下列有关该反应的说法中错误的是

A.断开1molX(g)和1molY(g)中的化学键,要吸收akJ能量
B.1molZ(g)和1molW(g)所具有的能量为bkJ
C.每生成1molZ(g)和1molW(g)吸收ckJ能量
D.升高温度,可加快该反应的速率
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置(气密性已检查)制备Fe(OH)2白色沉淀。
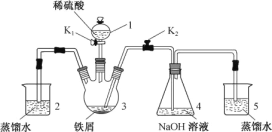
请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使溶液能进入4中________。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:
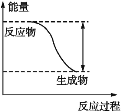
(1)该反应为_________(填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率增大,下列措施可行的是_________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度 D.使用催化剂
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为:_________(填“正”或“负”)极,该极上发生的电极反应为:_________,外电路中电子移动方向为:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吸热反应H2S(g)+CO2(g)![]() COS(g)+H2O(g),若在恒容绝热的容器中发生,下列情况下反应一定达到平衡状态的是
COS(g)+H2O(g),若在恒容绝热的容器中发生,下列情况下反应一定达到平衡状态的是
A.容器内的压强不再改变
B.容器内气体密度不再改变
C.容器内c(H2S):c(CO2):c(COS):c(H2O)=1:1:1:1
D.单位时间内,断开H-S键的数目和生成H-O键的数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第16届海南国际车展上:展出了中国研制的新型燃料电池汽车,该车装有“绿色心脏”---质子交换膜燃料电池。某种质子交换膜燃料电池如图所示。下列说法正确的是
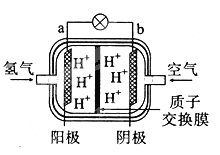
A.该电池的a极发生氧化反应B.正极反应为:O2+4e-+2H2O=4OH-
C.质子(H+)通过质子交换膜移动到a电极D.该燃料电池的能量转化率可达到100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌、鼓瑟齐鸣。璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应。鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色。请回答下列问题:
(1)火焰利用了部分金属元素特征的__________反应,该反应属于__________(填“物理”或“化学”)变化。
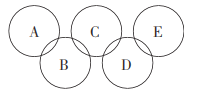
(2)如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含的电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为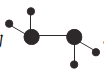 ,C可作光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,两元素的原子序数之比为2:1。根据以上信息回答下列问题:
,C可作光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,两元素的原子序数之比为2:1。根据以上信息回答下列问题:
①B的水溶液呈弱酸性,其主要的电离方程式可表示为___________________,D的化学式是___________________。
②A、B、E中均含有的一种元素为___________________(填元素名称)。
③E的电子式为___________________。
④液态B与液态E反应可生成一种气态单质和一种常见液体,1mol B参加反应放出热量Q kJ,其反应的热化学方程式为___________________。
⑤![]() 分子中的N原子有一对孤对电子,能发生反应:
分子中的N原子有一对孤对电子,能发生反应:![]() 。试写出E与足量盐酸发生反应的化学方程式:______________________________________。
。试写出E与足量盐酸发生反应的化学方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点232℃)与Cl2反应制备SnCl4,装置如下图所示。
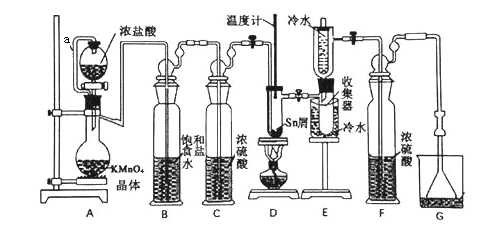
已知:①SnCl2、SnCl4有关物理性质如下表
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
②SnCl4遇水极易水解生成SnO2·xH2O。
回答下列问题:
(1)导管a的作用是__________,装置A中发生反应的离子方程式为_____________ 。
(2)当观察到装置F液面上方出现______ 现象时才开始点燃酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的有两点:加快氯气与锡反应和_________。
(3)若上述装置中缺少装置C(其它均相同),则D处具支试管中发生的主要副反应化学方程式为_______________________________。
(4)Cl2和Sn的反应产物有SnCl4和SnCl2,为了防止产品中带入过多的SnCl2,装置D可改为油浴加热来控制温度,该温度范围是________。
(5)制得的SnCl4产品中常含有SnCl2,可用如下方法测定产品纯度:先准确称量7.60g产品于锥形瓶中,再加过量的FeCl3溶液,发生反应:SnCl2+2FeCl3===SnCl4+2FeCl2,再用0.1000 mol·L—1 K2Cr2O7标准溶液滴定生成的Fe2+,此时还原产物为Cr3+,消耗标准溶液 20.00 mL,则SnCl4产品的纯度为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在工业上主要采用离子交换膜法电解饱和食盐水制取H2、Cl2、NaOH,请回答下列问题:
(1)在电解过程中,与电源正极相连的电极上发生的电极反应为__;
(2)电解之前食盐水需要精制,目的是除去粗盐中的Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有a:Na2CO3溶液,b:Ba(OH)2溶液,c:稀盐酸,其合理的加入顺序为___。
(3)如果在容积为10L的离子交换膜电解槽中,1min在阴极可产生标况下11.2L的H2,这时溶液中OH-的物质的量浓度为__;
(4)Cl2常用于自来水消毒杀菌,现有一种新型消毒剂ClO2,若它们在杀菌过程中的还原产物均为Cl-,消毒等量的自来水,所需的Cl2和ClO2的物质的量之比为:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃32mL与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数为( )
A.75%B.50%C.25%D.12.5%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com