
【题目】采用CO与H2反应合成再生能源甲醇,反应如下:CO(g)+ 2H2(g)![]() CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。则下列理解不符合题意的是
CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。则下列理解不符合题意的是
A. B点的速率比C点的大
B. A、B、C三点的平衡常数KA、KB、KC的大小关系为:KA=KB>KC
C. 若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为2L
D. 合成甲醇的反应为放热反应
【答案】A
【解析】A. B点到C点,升温反应速率增大,所以B点的速率比C点的小,故A不符合题意;B.升温平衡左移,K减小,所以 A、B、C三点的平衡常数KA、KB、KC的大小关系为:KA=KB>KC,故B符合题意;C. 平衡状态A时,c(CO)=0.5mol/L,c(H2)=1mol/L,c(CH3OH)=0.5mol/L,KA=![]() =1。平衡状态B时,设容器体积为xL,c(CO)=2/xmol/L,c(H2)=4/xmol/L,c(CH3OH)=8/xmol/L,KB=
=1。平衡状态B时,设容器体积为xL,c(CO)=2/xmol/L,c(H2)=4/xmol/L,c(CH3OH)=8/xmol/L,KB=![]() =KA=1,x=2,平衡状态B时容器的体积为2L,故C正确;D. 升温平衡左移,所以合成甲醇的反应为放热反应,故D正确。故选A。
=KA=1,x=2,平衡状态B时容器的体积为2L,故C正确;D. 升温平衡左移,所以合成甲醇的反应为放热反应,故D正确。故选A。


科目:高中化学 来源: 题型:
【题目】以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是( )
A. 现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
B. 28 g CO和22.4 L CO2中含有的碳原子数一定相等
C. 标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D. a g Cl2中有b个氯原子,则阿伏加德罗常数NA的数值可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中所列出的物质 , 属于 贴错了标签的是( )
选项 | A | B | C | D |
物质的化学式 | HNO3(浓) | 乙醇 | P4 | CCl4 |
危险警告标签 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉和纤维素不属于同分异构体的原因是 ( )
A. 组成的元素不同 B. 物理性质、化学性质不同
C. 组成的单糖单元数不相同 D. 分子结构不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】农业生产中用的波尔多液杀菌剂由硫酸铜和石灰乳按一定比例配制而成,它能防治植物病害的原因是( )
A.硫酸铜使菌体蛋白质盐析
B.石灰乳使菌体蛋白质水解
C.菌体蛋白质能溶解于波尔多液中
D.铜离子和石灰乳使菌体蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示。下列说法不正确的是
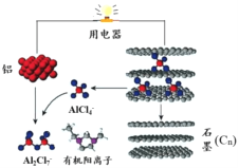
A. 放电时,铝为负极,石墨为正极
B. 放电时的负极反应为:Al-3e-+7AlCl4-===4Al2Cl7-
C. 充电时的阳极反应为:Cx+ AlCl4--e-===CxAlCl4
D. 放电时,有机阳离子向铝电极方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】杨梅醛是常用的水果型食用香精,合成路线如下。
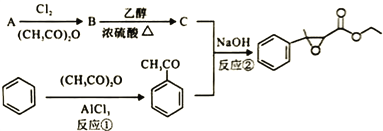
(1)杨梅醛的分子式为______________。
(2)与![]() 互为同分异构体的芳香醛有___________种,用于鉴别这些同分异构体的方法为___________。
互为同分异构体的芳香醛有___________种,用于鉴别这些同分异构体的方法为___________。
(3)反应①的反应类型为___________,该反应的另一产物在合成中可循环利用,其结构简式为___________。
(4)已知反应②的另一产物不含碳原子,B中含有的官能团为__________ (填名称),C的结构简式为___________。
(5)写出反应②的化学方程式___________。
(6)写出两种符合以下条件的杨梅醛的同分异构体的结构简式___________。
i.与FeCl3发生显色反应且能发生银镜反应
ⅱ.有三个互为间位的取代基且每个取代基含一个官能团
ⅲ含有-CH3和-CHO基团各两个
(7)根据上述合成路线写出乙酐和A为原料制备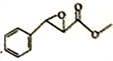 的合成路线____________(其试剂任选)。
的合成路线____________(其试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的回收利用是环保领域研究的热点课题。
(1)在太阳能的作用下,以CO2为原料制取炭黑的流程如右图所示,其总反应的化学方程式为_________。

(2)CO2经过催化氢化合成低碳烯烃.其合成乙烯的反应为2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g)△H,已知几种化学键键能如下表所示:(CO2的结构式:O=C=O)
CH2=CH2(g)+4H2O(g)△H,已知几种化学键键能如下表所示:(CO2的结构式:O=C=O)
物质 | H-H | C=O | C=C | C-H | H-O |
能量/kJmol-1 | 436 | 745 | 615 | 413 | 463 |
则△H=_________。
(3)在2L恒容密闭容器中充入2molCO2和n molH2,在一定条件下发生(2)中的反应,CO2的转化率与温度、投料比[X= ![]() ]的关系如图所示。
]的关系如图所示。

①X1_________X2(填“>”、“<”或“=”,下同),平衡常数KA_________KB.
②若B点的投料比为3,且从反应开始到B点需要10min,则v(H2)=_______ molL-1·min-1。
(4)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图如下图。(丙烯的结构简式:CH3CH=CH2)

①b电极的名称是_________;
②产生丙烯的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验的操作、现象和解释或结论都正确的是
操作 | 现象 | 解释或结论 | |
A | 将饱和Na2SO4溶液加入到饱和石灰中 | 有白色沉淀 | 说明Ksp[Ca(OH)2]大于Ksp[CaSO4] |
B |
| 试剂瓶中有一段稳定水柱 | 装置气密性良好 |
C | 将Al2(SO4)3溶液蒸干 | 有白色固体生成 | A13+水解生成Al(OH)3 |
D |
| 锥形瓶溶液产生淡黄色沉淀 | 苯与溴发生取代反应 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com