
根据要求填空:
(1)在0.1mol/L的CH3COOH溶液中,若加入少量的蒸馏水,溶液的pH ;若加入少量的纯醋酸,溶液中的c(CH3COO—) ;若加入少量的NaOH固体,溶液中的c(H+) ;若加入少量的CH3COONa固体,溶液中的c(OH—) 。(以上均用“增大”、“减小”或“不变”填空)
(2)在以KOH为电解质溶液的氢氧燃料电池中,电池工作时其负极的电极反应式为 正极的电极反应式为 。
(1)增大;增大;减小;增大。(2)2H2-4e—+4OH—=4H2O , O2+4e—+2H2O=4OH—
【解析】
试题分析:(1)对于0.1mol/L的稀CH3COOH溶液中,若加入少量的蒸馏水,电离平衡CH3COOH 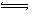 CH3COO-+H+.向正反应方向移动,使溶液的H+浓度增大,但水对离子的稀释作用大于平衡正向移动使离子浓度增大的趋势,总的来说C(H+)减小,所以溶液的pH增大。若加入少量的纯醋酸,由于C(CH3COOH)增大,平衡正向移动,使C(CH3COOH)减小,溶液中的c(CH3COO—)增大。若加入少量的NaOH固体,由于发生反应:H++OH-=H2O消耗了溶液中的H+,使c(H+)减小,平衡正向移动使c(H+)又有所增加,但消耗的浓度大于平衡增加的浓度,总的来说溶液中c(H+)减小。若加入少量的CH3COONa固体,溶液中的c(CH3COO—)增大,平衡逆向移动,溶液中c(H+)减小,c(OH—)增大。(2)以KOH为电解质溶液的氢氧燃料电池中,通入H2的电极为负极,电池工作时其负极的电极反应式为2H2-4e—+4OH—=4H2O,通入O2的电极为正极,正极的电极反应式为O2+4e—+2H2O=4OH—。总反应式为2H2+O2=2H2O。
CH3COO-+H+.向正反应方向移动,使溶液的H+浓度增大,但水对离子的稀释作用大于平衡正向移动使离子浓度增大的趋势,总的来说C(H+)减小,所以溶液的pH增大。若加入少量的纯醋酸,由于C(CH3COOH)增大,平衡正向移动,使C(CH3COOH)减小,溶液中的c(CH3COO—)增大。若加入少量的NaOH固体,由于发生反应:H++OH-=H2O消耗了溶液中的H+,使c(H+)减小,平衡正向移动使c(H+)又有所增加,但消耗的浓度大于平衡增加的浓度,总的来说溶液中c(H+)减小。若加入少量的CH3COONa固体,溶液中的c(CH3COO—)增大,平衡逆向移动,溶液中c(H+)减小,c(OH—)增大。(2)以KOH为电解质溶液的氢氧燃料电池中,通入H2的电极为负极,电池工作时其负极的电极反应式为2H2-4e—+4OH—=4H2O,通入O2的电极为正极,正极的电极反应式为O2+4e—+2H2O=4OH—。总反应式为2H2+O2=2H2O。
考点:考查燃料电池电极式的书写及外界条件对弱电解质电离平衡、离子浓度溶液酸碱性的影响的知识。


科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液 体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 21.48 |
| 第二次 | 10.00 | 4.00 | 25.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:





 的结构简式
的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
 (2013?江西模拟)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室中模拟上述过程.其设计的模拟装置如图:
(2013?江西模拟)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室中模拟上述过程.其设计的模拟装置如图:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com