


分析 A、B、C、D均为含两个碳原子的有机化合物,其中D是一种最常见食用有机酸,则D为CH3COOH,逆推可知C为CH3CHO,B为CH3CH2OH,在A与氢氧化钠水溶液、加热条件下反应得到的混合液中加过量的稀硝酸后再加硝酸银溶液产生白色沉淀,说明A中含有Cl元素,故A为CH3CH2Cl.
解答 解:A、B、C、D均为含两个碳原子的有机化合物,其中D是一种最常见食用有机酸,则D为CH3COOH,逆推可知C为CH3CHO,B为CH3CH2OH,在A与氢氧化钠水溶液、加热条件下反应得到的混合液中加过量的稀硝酸后再加硝酸银溶液产生白色沉淀,说明A中含有Cl元素,故A为CH3CH2Cl.
(1)A为CH3CH2Cl,A的分子式:C2H5Cl,C为CH3CHO,结构式为: ,
,
故答案为:C2H5Cl; ;
;
(2)反应①的方程式为:CH3CH2Cl+NaOH$→_{△}^{水}$ CH3CH2OH+NaCl,
B与D在一定条件下发生的反应:CH3CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
故答案为:CH3CH2Cl+NaOH$→_{△}^{水}$ CH3CH2OH+NaCl;CH3CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
点评 本题考查有机物的推断,涉及卤代烃、醇、醛、羧酸、酯的性质与转化,比较基础,注意根据醇的连续氧化反应进行推断,熟练掌握官能团的性质.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:选择题
| A. | 已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 | |
| B. | 对于CaCO3(s)═CaO(s)+CO2(g) 任何温度下都不能自发进行 | |
| C. | 实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键 | |
| D. | 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol. CO(g)+$\frac{1}{2}$O2(g)═CO2(g),△H=-283.0 kJ/mol. C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol. 则4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑨ | ||||
| 3 | ① | ② | ③ | ⑦ | ⑧ |
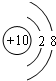 .
.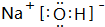 (填电子式),其所含有的化学键类型有离子键、极性共价键(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).
(填电子式),其所含有的化学键类型有离子键、极性共价键(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).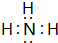 ,其水溶液呈碱性(填“酸性”、“中性”或“碱性”).
,其水溶液呈碱性(填“酸性”、“中性”或“碱性”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用热的纯碱水洗涤油污 | |
| B. | 用食醋消除暖水瓶中的水垢 | |
| C. | 用碘水来检测成熟的苹果中是否含有淀粉 | |
| D. | 纤维素在人体内可水解为葡萄糖,故可作为人类的营养物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若能与金属钠和碳酸氢钠反应,则其结构中同时含有-OH和-COOH | |
| B. | 若该物质中含有两个-CH3,则它可以是碳酸酯 | |
| C. | 若该物质中结构中不能只含有C-O键和C-H键 | |
| D. | 若1mol C3H6O3与足量钠反应只产生1mol氢气,说明一分子C3H6O3中含有2个-OH和一个-CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸与NaOH溶液反应的离子方程式为:H++OH-═H2O | |
| B. | 金属钠与乙醇反应的化学方程式为:2Na+2CH3CH2OH→2CH3CH2ONa+H2↑ | |
| C. | 聚氯乙烯的结构简式为: | |
| D. | 工业上制取Cl2的离子方程式为:2Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
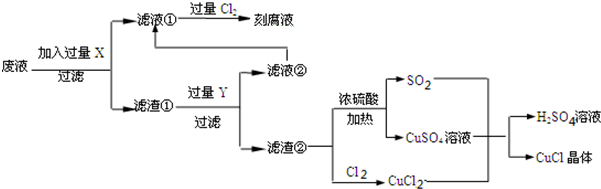
| 1 | 2 | 3 | |
| 空白试验消耗硫酸铈标准溶液的体积(ml) | 0.75 | 0.50 | 0.80 |
| 0.25克样品消耗硫酸铈标准溶液的体积(ml) | 24.65 | 24.75 | 24.70 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com