
科目:高中化学 来源:不详 题型:单选题
| A.24n(A1)+35.5n(Na)=W2—W1 | B.n(Na)+3n(A1)=aV2 |
| C.n(Na)+3n(A1)=V1/11.2 | D.aV2=V1/22.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.④⑤ | B.①⑤ | C.①②③ | D.①④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.NaOH的浓度为0.6 mol/L | B.在a点处溶液中的溶质为NaCl |
| C.在b点处溶液中的溶质只有NaAlO2 | D.图中线段oa : ab=5 : 1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.8.9g | B.9.0g | C.13.5g | D.27.0g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Fe+Al2O3,反应发生时放出大量的热。仔细阅读上述信息回答下列问题:
2Fe+Al2O3,反应发生时放出大量的热。仔细阅读上述信息回答下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
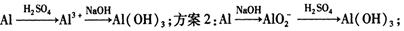
 o
o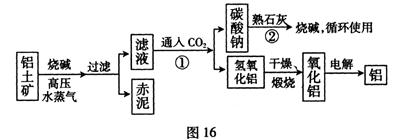
| | Al2O3 | Fe2O3 | 其他杂质 |
| 铝土矿 | 55% | 16% | — |
| 赤泥 | 15% | 48% | 一 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下与足量18mol/LH2SO4反应,最多可放出0.6 mol H2 |
| B.常温下与足量2mol/LHNO3反应,最少可放出0.45 mol H2 |
| C.常温下与足量2 mol/L H2SO4反应,放出H2的量在0.45 mol~0.6 mol之间 |
| D.常温下与足量2mol/LNaOH反应,放出H2的量在0.45 mol~0.6 mol之间 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.右边加0.9g Al | B.左边加0.98g Mg |
| C.左边加14.4g Mg,右边加15.3g Al | D.左边加14.4g Mg,右边加14.85g Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com