
下列说法正确的是( )
A.水的电离方程式:H2O H++OH-
H++OH-
B.升高温度,水的电离程度增大
C.在NaOH溶液中没有H+
D.在HCl溶液中没有OH-
科目:高中化学 来源:2014年高二化学人教版选修四 19一次电池 二次电池练习卷(解析版) 题型:选择题
已知蓄电池在放电时起原电池的作用,在充电时起电解池的作用。汽车上用的铅蓄电池是以一组充满海绵状灰铅的铅板和另一组结构相似的充满二氧化铅的铅板组成。两个电极用稀硫酸作电解质溶液。在放电时,两极发生的反应可分别表示为:
Pb+S-2e- PbSO4
PbSO4
PbO2+4H++S+2e- PbSO4+2H2O
PbSO4+2H2O
充电时,两极发生的反应分别表示为:
PbSO4+2e- Pb+S
Pb+S
PbSO4+2H2O-2e- PbO2+4H++S
PbO2+4H++S
则在放电时,下列说法中正确的是( )
A.充满海绵状灰铅的铅板为电源正极
B.充满二氧化铅的铅板为电源负极
C.铅板在放电时发生氧化反应
D.铅板在放电时发生还原反应
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 15盐类水解的原理练习卷(解析版) 题型:选择题
关于盐类水解的实质,下列叙述正确的是( )
A.盐的电离平衡被破坏B.水的电离平衡被破坏
C.没有中和反应发生D.溶液的pH一定变大
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 13pH的计算练习卷(解析版) 题型:选择题
常温下,柠檬酸水溶液的pH是3,食用醋的pH是2,可乐的pH是6,三种物质的溶液中c(OH-)分别是( )
A.1×10-11 mol·L-1,1×10-12 mol·L-1,1×10-8 mol·L-1
B.1×10-11 mol·L-1,1×10-8 mol·L-1,1×10-12 mol·L-1
C.2×10-11 mol·L-1,1×10-10 mol·L-1,1×10-8 mol·L-1
D.1×10-8 mol·L-1,1×10-11 mol·L-1,1×10-12 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 12水的电离 溶液的酸碱性练习卷(解析版) 题型:选择题
常温下,在0.01 mol·L-1硫酸溶液中,水电离出的氢离子浓度是( )
A.5×10-13 mol·L-1B.0.02 mol·L-1
C.1×10-7 mol·L-1D.1×10-12 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 11弱电解质的电离练习卷(解析版) 题型:选择题
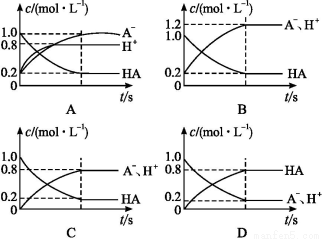
一元弱酸HA(aq)中存在下列电离平衡:HA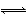 A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 10化学反应进行的方向练习卷(解析版) 题型:填空题
有A、B、C、D四个反应:
反应ABCD
ΔH/(kJ·mol-1)10.51.80-126-11.7
ΔS/(J·mol-1·K-1)30.0-113.084.0-105.0
则在任何温度下都能自发进行的反应是 ;任何温度下都不能自发进行的反应是 ;另两个反应中,在温度高于 ℃时可自发进行的反应是 ;在温度低于 ℃时可自发进行的反应是 。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 模块综合检测练习卷(解析版) 题型:选择题
下列关于工业生产的说法中,错误的是( )。
A.氯碱工业中的阳离子交换膜阻止阳离子通过
B.生产普通玻璃的主要原料有石灰石、石英和纯碱
C.工业上将粗铜进行精炼,应将粗铜连接在电源的正极
D.工业上,用焦炭在电炉中还原二氧化硅得到含少量杂质的粗硅
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 3单元综合检测练习卷(解析版) 题型:选择题
下图所示各烧杯中盛有海水,铁在其中被腐蚀的速率由快到慢的顺序为( )。
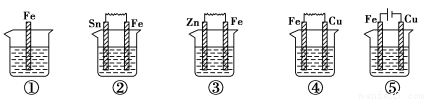
A.⑤②①③④ B.④③①②⑤ C.⑤④②①③ D.③②④①⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com