
硫代硫酸钠(Na2S2O3)俗称保险粉,可用于照相业作定影剂,也可用于纸浆漂白
作脱氯剂等。实验室可通过如下反应制取:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。
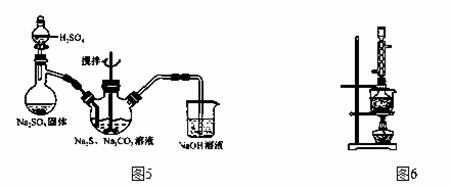
(1)用图5所示装置制取Na2S2O3,其中NaOH溶液的作用是 ▲ 。如将分液漏斗中的H2SO4
改成浓盐酸,则三颈烧瓶内除Na2S2O3生成外,还有 ▲ (填化学式)杂质生成。
(2)为测定所得保险粉样品中Na2S2O3·5H2O的质量分数,可用标准碘溶液进行滴定,反
应方程式为2Na2S2O3+I2=2NaI+Na2S4O6。
①利用KIO3、KI和HCl可配制标准碘溶液。写出配制时所发生反应的离子方程式: ▲ 。
②准确称取一定质量的Na2S2O3·5H2O样品于锥形瓶中,加水溶解,并滴加 ▲ 作
指示剂,滴定终点的现象是 ▲ 。
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则测量的Na2S2O3·5H2O的
质量分数会 ▲ (填“偏高”、“偏低”或“不变”)。
(3)本实验对Na2S的纯度要求较高,利用图6所示的装置可将工业级的Na2S提纯。已知Na2S
常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯步骤依次为:
①将已称量好的工业Na2S放入圆底烧瓶中,并加入一定质量的酒精和少量水;
②按图6所示装配所需仪器,向冷凝管中通入冷却水,水浴加热;
③待烧瓶中固体不再减少时,停止加热,将烧瓶取下;
④趁热过滤;
⑤ ▲ ;
⑥将所得固体洗涤、干燥,得到Na2S·9H2O晶体。
科目:高中化学 来源: 题型:
下列实验过程中,始终无明显现象的是 ( )
A.NO2通入FeSO4溶液中
B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中
D.SO2通入已酸化的Ba(NO3)2溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
电浮选凝聚法处理污水的原理如图所示。电解过程生成的胶体能使污水中的悬浮物凝聚成团而除去,电解时阳极也会产生少量气体。下列说法正确的是
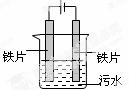 A.可以用铝片或铜片代替铁片
A.可以用铝片或铜片代替铁片
B.阳极产生的气体可能是O2
C.电解过程中H+向阳极移动
D.若污水导电能力较弱,可加入足量硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的数值,下列说法正确的是
A.23gNO2和N2O4的混合气体中含有的氮原子数为0.5NA
B.4.2 g丙烯中所含的共用电子对总数为0.6NA
C.过氧化氢分解制得标准状况下1.12 L O2,转移电子数目为 0.2 NA
D.在高温、高压、催化剂的条件下,28gN2和6gH2充分反应,生成NH3的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,有①氨水、②NH4Cl溶液、③Na2CO3溶液、④NaHCO3溶液各25mL,物质的
量浓度均为0.1mol·L−1,下列说法正确的是
A.四种溶液的pH的大小顺序:①>④>③>②
B.将溶液①、②等体积混合所得碱性溶液中:c(NH4+)<c(NH3·H2O)
C.向溶液①、②中分别滴加25mL 0.1mol·L−1盐酸后,溶液中c(NH4+):①<②
D.将溶液③、④等体积混合所得溶液中:
2c(OH−)-2c(H+)=3c(H2CO3)+c(HCO3-)-c(CO32−)
查看答案和解析>>
科目:高中化学 来源: 题型:
利用下列实验装置不能完成相应实验的是 ( )。
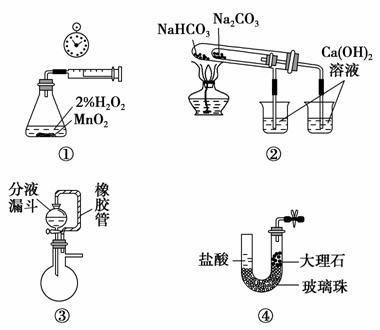
A.用装置①测量生成 氧气的化学反应速率
氧气的化学反应速率
B.用装置②比较NaHCO3和Na2CO3的热稳定性
C.装置③中分液漏斗内的液体可顺利加入蒸馏烧瓶
D.装置④可实现制取CO2实验中的“即关即止,即开即用”的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如下图所示。
(1)由图中所给数据进行分析,该反应的化学方程式为 。
(2)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为_______。
(3)达到平衡是X的浓度是 ;
(4)当反应进行到第 min,该反应达到平衡。反应达到平衡后,下列措施能加快化学反应速率的有_____________
A.增大反应物的浓度 B.升高温度 C.使用正催化剂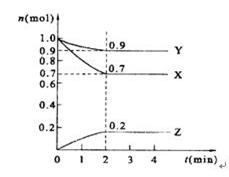
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时弱电解质电离平衡常数:Ka(CH3COOH)=1.8×10—5,Ka(HSCN)=0.13。
(1)将20 mL 0.10 mol/L CH3COOH溶液和20 mL 0.10 mol/L的HSCN溶液
分别与0.10 mol/L的NaHCO3溶液反应,实验测得产生CO2气体体积V
与时间t的关系如图甲所示:


反应开始时,两种溶液产生CO2的速率明显不同的原因是____________
_________________________________________________;反应结束后所得溶液中c(SCN—)______c(CH3COO—) (填“>”、“=”或“<”)。
(2)2.0×10—3 mol/L的HF水溶液中,调节溶液pH(忽略调节pH时溶液的
体积变化),测得平衡体系中c(F—)、c(HF)与溶液pH的关系如图乙所示。
则25℃时,HF电离平衡常数为Ka(HF)=_____________________________
______________________(列式并求值,不写单位)。
(3)难溶物CaF2溶度积常数(Ksp)= 1.5×10—10,将4.0×10—4mol/L的HF溶液
与4.0×10—4mol/L的CaCl2溶液等体积混合,调节溶液pH=4(忽略调节
pH时溶液的体积变化),试分析混合后是否有沉淀生成?________(填“有”
或“没有”),简述理由:__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com