
| A. | 湿法冶铜:Fe+CuSO4═FeSO4+Cu | |
| B. | 高炉炼铁:Fe2O3+3CO═2Fe+3CO2 | |
| C. | 制氧气:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | |
| D. | 制环氧乙烷:2C2H2( 乙炔)+O2$\frac{\underline{\;催化剂\;}}{加热}$2C2H4O ( 环氧乙烷) |
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:多选题
| A. | 在配制前用稀硫酸润洗容量瓶后,未用蒸馏水洗涤 | |
| B. | 定容摇匀后,发现液面低于刻度线,再加入蒸馏水至与刻度线相切 | |
| C. | 洗涤量筒,并将洗涤液转入容量瓶 | |
| D. | 定容时仰视读数. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
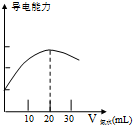 某学习小组用DIS系统测定食用白醋中醋酸的物质的量浓度,以溶液的导电能力来判断滴定终点.实验步骤如下:
某学习小组用DIS系统测定食用白醋中醋酸的物质的量浓度,以溶液的导电能力来判断滴定终点.实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40K和40Ca原子中的质子数和中子数都相等 | |
| B. | 任何元素的原子都是由核外电子和核内中子、质子组成的 | |
| C. | 具有相同核电荷数的粒子,一定是同种原子的微粒 | |
| D. | 同种元素的不同核素之间互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 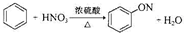 | |
| B. | H2C=CH2+Br2→CH3CHBr2 | |
| C. | CH3COOH+CH3CH2OH $→_{△}^{浓硫酸}$ CH3CH2OCH2CH3+H2O | |
| D. | CH4+2O2 $\stackrel{点燃}{→}$ CO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、Cl-、CO32- | B. | NH4+、Na+、Cl-、SO42- | ||
| C. | Na+、HCO3-、NO3-、SO42- | D. | K+、MnO4-、Na+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
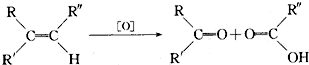 ,现有二烯烃C10H18与KMnO4溶液作用后可得到三种有机物:( CH3)2CO、CH3COOH、CH3CO(CH2)2COOH,由此推断二烯烃可能的结构简式为(CH3)2C═CHCH2CH2C(CH3)═CHCH3.
,现有二烯烃C10H18与KMnO4溶液作用后可得到三种有机物:( CH3)2CO、CH3COOH、CH3CO(CH2)2COOH,由此推断二烯烃可能的结构简式为(CH3)2C═CHCH2CH2C(CH3)═CHCH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
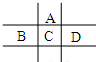 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com