
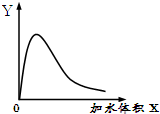
 一定温度下对冰醋酸逐滴加水稀释,发生如图变化,图中Y轴的含义可能是( )
一定温度下对冰醋酸逐滴加水稀释,发生如图变化,图中Y轴的含义可能是( )| A、导电能力 | B、pH |
| C、氢离子浓度 | D、溶液密度 |


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
 NOx是汽车尾气中的主要污染物之一.通过NOx传感器可监测NOx的含量,其工作原理示意图如下.下列说法正确的是( )
NOx是汽车尾气中的主要污染物之一.通过NOx传感器可监测NOx的含量,其工作原理示意图如下.下列说法正确的是( )| A、Pt电极作负极,NiO电极作正极 |
| B、Pt电极上发生的是氧化反应 |
| C、NiO电极上发生的是还原反应 |
| D、NiO电极的电极反应式为NO+O2--2e-═NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 .现有乙酰水杨酸的粗品,某同学用中和法测定产品纯度:取a g产品溶解于V1 mL 1mol/L的NaOH溶液中,加热使乙酰水杨酸水解,再用1mol/L的盐酸滴定过量的NaOH,当滴定终点时消耗盐酸V2 mL;
.现有乙酰水杨酸的粗品,某同学用中和法测定产品纯度:取a g产品溶解于V1 mL 1mol/L的NaOH溶液中,加热使乙酰水杨酸水解,再用1mol/L的盐酸滴定过量的NaOH,当滴定终点时消耗盐酸V2 mL;查看答案和解析>>
科目:高中化学 来源: 题型:
| A、I- |
| B、HCO3- |
| C、Fe2+ |
| D、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol | B、4mol |
| C、6mol | D、8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓盐酸与铁屑反应:2Fe+6H+═2 Fe3++3H2↑ |
| B、钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ |
| C、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 【实验方案】 | 【现象】 | 【结论】 |
| ①分别取等量的热水和冷水于试管中 分别加入CuSO4固体 |
CuSO4固体在热水中溶解较快 | 温度越高,固体溶解速率越快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COOH的电离平衡常数增大为原来的10倍 |
| B、CH3COO-与CH3COOH的浓度之比增大为原来的10倍 |
| C、CH3COO-与H+的浓度之积减小为原来的0.1 |
| D、CH3COOH与CH3COO-的浓度之和减小为原来的0.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com