
| A、0.1 mol?L-1的NaCl溶液 |
| B、pH=6的醋酸用水稀释100倍 |
| C、pH=10的氢氧化钠溶液稀释1000倍 |
| D、0.1 mol?L-1的硫酸100 mL跟0.2 mol?L-1 NaOH溶液150 mL完全反应 |
| 0.2mol/L×0.05L |
| 0.25L |
| 10-14 |
| 0.04mol/L |


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
| A、MgSO4 |
| B、NaAlO2 |
| C、AlCl3 |
| D、FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、对应简单离子半径:X>W |
| B、对应气态氢化物的稳定性Y>Z |
| C、化合物XZW既含离子键,又含共价键 |
| D、Y的氧化物能与Z的氢化物和X的最高价氧化物对应的水化物的溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
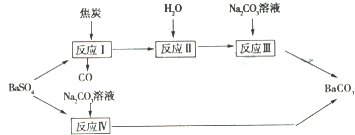
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaNO3、NH3?H2O、N2 |
| B、Fe、CH3COOH、液氯 |
| C、漂白粉、BaSO4、CO2 |
| D、Ba(OH)2、HF、酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、干馏煤可以得到甲烷、苯和氨等重要化工原料 |
| B、人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
| C、用大米酿的酒在一定条件下密封保存,时间越长越香醇 |
| D、淀粉在人体内水解的最终产物为葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝是地壳中含量最多的金属元素 |
| B、硅单质是生产光导纤维的重要原料 |
| C、硅酸盐产品有陶瓷、玻璃、水泥等 |
| D、黄铜比纯铜的硬度大 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com