
����Ŀ��ij�¶�ʱ��Ag2SO4��ˮ��Һ�е��ܽ�ƽ��������ͼ��ʾ������˵������ȷ����(����)
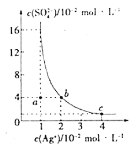
A.b���Ӧ��Ksp(Ag2SO4)����c���Ӧ��Ksp(Ag2SO4)
B.��ȡ�����ܼ��ķ�������ʹa���Ӧ����Һ��Ϊb���Ӧ����Һ
C.���¶��£�Ksp(Ag2SO4)=1.6��10-5
D.0.02molL-1��AgNO3��Һ��0.2molL-1��Na2SO4��Һ�������ϲ������ɳ���
���𰸡�B
��������
A���¶�һ��ʱ���ܽ�ƽ������������㶼����������Һ��Ksp����ȣ���A��ȷ��
B��������Һ��Ag+Ũ�Ⱥ�SO42-Ũ�ȶ���������Ϊa��ﵽb�㣬��B����
C����ͼ���֪��Ag2SO4���ܶȻ�����Ksp=(0.02)2��0.04=1.6��10-5((molL-1)2)����C��ȷ��
D��0.02mol/L��AgNO3��Һ��0.2mol/L��Na2SO4��Һ�������ϣ�c(Ag+)=0.01moL/L��c(SO42-)=0.1mol/L����C���֪Ag2SO4���ܶȻ�����Ksp=(0.02)2��0.04=1.6��10-5((molL-1)2)����(0.01)2��0.1=1��10-5��1.6��10-5��û�г������ɣ���D��ȷ��
��ѡB��


 ��У������Ԫͬ��ѵ��������ϵ�д�
��У������Ԫͬ��ѵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����仯������������;��������ʵ������������±���ʾ��
|
|
|
|
|
| |
�۵�/�� | -85.5 | 115.2 | >600 | -75.5 | 16.8 | 10.3 |
�е�/�� | -60.3 | 444.6 | ���ֽ⣩ | -10.0 | 45.0 | 337.0 |
�ش��������⣺
��1�����ݼ۲���ӶԻ������ۣ�![]() ��
��![]() ��
��![]() ����̬�����У�����ԭ�Ӽ۲���Ӷ�����ͬ���������ӵ���__________��
����̬�����У�����ԭ�Ӽ۲���Ӷ�����ͬ���������ӵ���__________��
��2����̬���������Ե�������ʽ���ڣ�����ӵ����幹��Ϊ__________�Σ����й��ۼ���������__________�֣��������������д�����ͼ��ʾ�����۷��ӣ��÷�����![]() ԭ�ӵ��ӻ��������Ϊ__________��
ԭ�ӵ��ӻ��������Ϊ__________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���绯ѧԭ���ڷ�ֹ������ʴ������ת���ȷ���Ӧ�ù㷺��
(1)�ٸ����ں�ˮ���������绯ѧ��ʴ��������Ӧʽ��__________��
��ͼ�У�Ϊ������բ�ŵĸ�ʴ������B����ѡ��__________(����Zn������Cu��)��
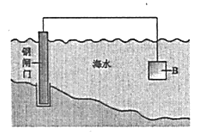
(2)��ͼΪ��������ģ��ʵ��װ�ã�������__________��������������Ч���ķ����ǣ�ȡ�������缫��������Һ���Թ��У�_________����˵������Ч���á�
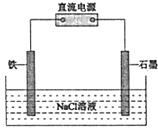
(3)����ȼ�ϵ����һ�����͵Ļ�ѧ��Դ���乹����ͼ��ʾ��
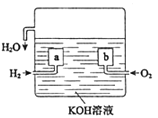
a��bΪ���ʯī�缫��ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ硣
��a�ĵ缫��Ӧʽ��_________��
������ع�����3.6gˮ�����·��ͨ����_______mol�ĵ��ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ��ʯ��Ҫ��������ͭ(Cu2S)��������FeO��CaO��SiO2�ȡ��Ի�ͭ��ʯΪԭ���Ʊ�CuCl2��2H2O�Ĺ���������ͼ��ʾ��

��֪����.��������[c0(Mn+)=0.1mol��L-1]�γ��������������pH��Χ���£�
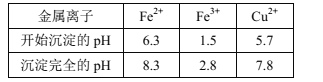
��.NaCl������ˮ�������ھƾ������¶ȱ仯�ܽ�ȱ仯�����ԣ�CuCl2��H2O������ˮ���ƾ���Ũ��ˮ�����¶������ܽ�ȱ仯��������
��.Ksp(CaF2)=4.0��10-11
��1��Ϊ����ߡ��ܽ���Ч�ʣ��ɲ�ȡ�Ĵ�ʩ��___��д�����ܽ���������Cu2S�ܽ�ʱ���ӷ���ʽ��___��
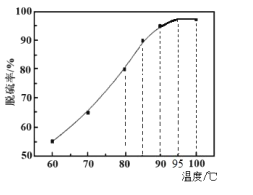
��2��������ʱ�������¶ȵ����ߣ������ʳ��������ƣ���ͼ����ԭ����___��
��3��д�����ѷ���ʱHF������Ӧ�Ļ�ѧ����ʽ��___��
��4��������������������NaClO������������___��
��5��������X���ľ��������___��
��6������������X����ĸҺ����һϵ�в����ɵõ�����һ�����ʣ�Ҫ�õ����ִ�������ѡ�������Լ�ϴ��___��
A��Ũ���� B��ˮ C���ƾ� D��Ũ��ˮ
��7������Һ���м���NaF��ȥ��Һ��Ca2+(Ũ��Ϊ1.0��10-3mol��L-1)������Һ��c(F-)=2.0��10-3mol��L-1ʱ��������Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п(ZnFe2O4)�ǶԿɼ������еİ뵼���������ʵ�����Ʊ�ԭ��Ϊ��
��ZnSO4+2FeSO4+3Na2C2O4+6H2O![]() ZnFe2(C2O4)3��6H2O��+3Na2SO4
ZnFe2(C2O4)3��6H2O��+3Na2SO4
��ZnFe2(C2O4)3��6H2O![]() ZnFe2O4+2CO2 ��+4CO��+6H2O
ZnFe2O4+2CO2 ��+4CO��+6H2O
�ش���������:
(1)��̬ Fe2+�ļ۲�����Ų�ͼΪ___________.
(2)�����ܴ�С�Ƚϣ�I1(Zn)___________ I1(Cu)��I2(Zn)___________ I2 (Cu) (����>����<������=��)��
(3)Na2SO4 �������ӵĿռ乹����___________���������� S ���ӻ�������_____��
(4)CO��N2�ķ��ӽṹ���ƣ���״���£�VLCO2��CO�Ļ�������к��������ʵ���Ϊ___________����CO2��Ϊ�ȵ������������____________(дһ�ּ���)��
(5)ZnCl2��ZnBr2��ZnI2 ���۵�����Ϊ283����394����446��������Ҫԭ����___________��
(6)����̼��ɵ�ij�־���ľ�����ͼ��ʾ����������ԭ�����������������塣

��֪�þ�����ܶ�Ϊ dg��cm-3��NA �ǰ����ӵ�������ֵ��
�ٸþ�����Fe��Cԭ�ӵ�����Ϊ___________��
�ڸþ���������������������ԭ������ĺ˼���� D=___________nm(ֻ�м���ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾʵ��װ�ã��ܴﵽ��Ӧʵ��Ŀ�Ļ�����������ȷ���ǣ� ��
A.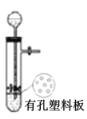 ��ʾװ������ Cu ��Ũ H2SO4 ��ȡ������ SO2 ����
��ʾװ������ Cu ��Ũ H2SO4 ��ȡ������ SO2 ����
B.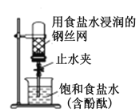 ��ͼ�е�ֹˮ�У�һ��ʱ��ɹ۲쵽�ձ�����Һ�������Թ���
��ͼ�е�ֹˮ�У�һ��ʱ��ɹ۲쵽�ձ�����Һ�������Թ���
C.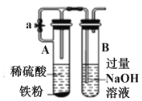 ����ͼ��ʾװ����ȡ Fe(OH)2
����ͼ��ʾװ����ȡ Fe(OH)2
D.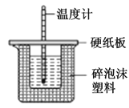 ����ͼ�ⶨ�кͷ�Ӧ��Ӧ��
����ͼ�ⶨ�кͷ�Ӧ��Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������һ���ܿ�������պ��ͷ������IJ��ϡ�LaNi5�Ͻ�NaBH4��H3B-NH3��Mg2NiH4�ȶ���DZ�ڴ�����ϡ��ش��������⣺
��1����̬Niԭ�ӵĺ�������Ų�ʽΪ____����___________��δ�ɶԵĵ��ӣ�
��2��NaBH4��HΪ-1�ۣ�Na��B��H�縺���ɴ�С��˳����_________��BH4-���ӵ����幹��Ϊ________������B���ӻ��������Ϊ_____��
��3��B2H6��NH3���Ͽ�������H3B-NH3��H3B-NH3����ʱ������Ӧ��H3B-NH3��BN+3H2�������ͷų�H2��BN��������ʯī�Ľṹ��B2H6��NH3��BN�ķе��ɸߵ��͵�˳��Ϊ_________�� ԭ����___��
��4��X-�����������������Mg2NiH4 ���������������ĺͶ������Niԭ��ռ�ݣ�����Mgԭ�ӵ�Ni��λ������ȡ���Mgԭ��������Niԭ���γɵ�_____��϶�У�������塱�����塱�������϶ռ�аٷ���Ϊ_____��
��5����֪Mg2NiH4 ����ľ�������Ϊ646.5 pm��Һ����ܶ�Ϊ0.0708 g��cm-3�����Բ���������ܶ���Һ̬���ܶ�֮�ȶ��崢����ϵĴ�����������Mg2NiH4 �Ĵ���������Һ���___�����г�����ʽ���ɣ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���᳦��ҩ�����Ч�ɷֵĺϳ�·����ͼ��ʾ(�����Լ��ͷ�Ӧ��������ȥ)��

��ش��������⣺
��1��E�к��еĹ�����Ϊ__��
��2���ڵķ�Ӧ������__��
��3�����жԿ��᳦��ҩ�����Ч�ɷֿ��ܾ��е������Ʋⲻ��ȷ����__(����ĸ)��
a.ˮ���Աȱ��ӵĺã��ܶȱȱ��ӵĴ�
b.�ܷ�����ȥ��Ӧ
c.�ܷ����Ӿ۷�Ӧ
d.�������������
��4���ٵķ�Ӧ����ʽΪ__��
��5����������������E��ͬ���칹����__�֡�д�����к˴Ź����������������Ľṹ��ʽ��__��
a.��E������ͬ�Ĺ������ҹ����Ų���ͬһ������
b.ˮ�����֮һ�����Ȼ�����Һ������ɫ��Ӧ
��6����������ı�����������һ��ȡ����ʱ����ȡ������ڡ���λ�ϵ���ԭ�ӣ��������Ȼ��ı�����������һ��ȡ����ʱ����ȡ���Ȼ���λ�ϵ���ԭ�ӡ��ݴ���Ƴ���AΪԭ�Ϻϳ�![]() ��·��(�������п��᳦��ҩ�����Ч�ɷֵĺϳ�·�߽��д���)___��
��·��(�������п��᳦��ҩ�����Ч�ɷֵĺϳ�·�߽��д���)___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ���������ʹ㷺���ڽ�������װ���ϵȣ���ϩ���Ǻϳɱ�ϩ������ԭ��֮һ����ϩ���������������͡����ϵȡ��Ա�ϩȩΪԭ��������ϩ������ϩ���������ͼ��ʾ��
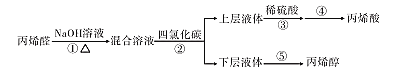
��֪��
��2CH2=CH-CHO+NaOH![]() CH2=CHCH2OH+CH2=CHCOONa
CH2=CHCH2OH+CH2=CHCOONa
��2CH2=CHOONa+H2SO4��2CH2=CHCOOH+Na2SO4
���й����ʵ�������������
���� | ��ϩȩ | ��ϩ�� | ��ϩ�� | ���Ȼ�̼ |
�е�/�� | 53 | 97 | 141 | 77 |
�۵�/�� | - 87 | - 129 | 13 | -22.8 |
�ܶ�/g��mL-3 | 0.84 | 0.85 | 1.02 | 1.58 |
�ܽ���(����) | ������ˮ���л��ܼ� | ����ˮ���л��ܼ� | ����ˮ���л��ܼ� | ������ˮ |
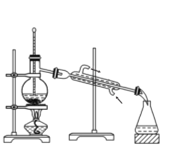
(1)��������Ҫ��������30min������װ����ͼ��ʾ������L������________��
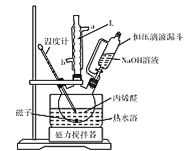
(2)������ʹ�õ���Ҫ�����Ƿ�Һ©������ʹ��֮ǰ����еIJ����� ___��
(3)�����ܰ���____�����ˡ���ˮϴ�ӡ��������ɡ�
(4)�������У����������²�Һ�塱����������Ȼ�̼���ٷ������ϩ��(��ͼ)��Ҫ�õ���ϩ��Ӧ�ռ� ____(���¶�)����֡�ͼ����һ�����Դ���Ӧ��Ϊ____��
(5)�ⶨ��ϩ����Ħ��������ȷ��ȡamL��ϩ���ڷ�Һ©���У���ƿ��ʢװ����������ʵ��ǰ������B�ж���Ϊb mL������ϩ����ȫ��Ӧ����ȴ�����¡���ƽB��CҺ�棬������B�Ķ���Ϊc mL����֪����������Ħ�����ΪVL��mol-1��
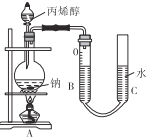
��ƽB��CҺ��IJ�����____��ʵ���ñ�ϩ����Ħ������Ϊ____g��mol-1(�ô���ʽ��ʾ)���������ʱC��Һ�����B�ܣ���ý����____(�ƫ��ƫС�����䡱)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com