
| A. | 第六周期第ⅢA族的元素Tl,其氢氧化物的碱性比Al(OH)3弱 | |
| B. | 卤族元素At的单质为有色固体,AgAt可能不溶于水也不溶于稀硝酸 | |
| C. | Li与水反应比钠与水反应剧烈 | |
| D. | H2Se是无色,有毒,比H2S稳定的气体 |
分析 A.同一主族元素,元素的金属性随着原子序数增大而增强,元素的金属性越强,其最高价氧化物的水化物碱性越强;
B.卤素单质都是有色物质,且随着原子序数增大其单质颜色加深,AgX中只有AgF易溶于水,其它卤化银既不属于水也不溶于稀硝酸;
C.元素的金属性越强,其单质与水或酸反应越剧烈;
D.元素的非金属性越强,其氢化物的稳定性越强.
解答 解:A.同一主族元素,元素的金属性随着原子序数增大而增强,元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性Tl>Al,所以氢氧化物的碱性比Al(OH)3强,故A错误;
B.卤素单质都是有色物质,且随着原子序数增大其单质颜色加深,AgX中只有AgF易溶于水,其它卤化银既不属于水也不溶于稀硝酸,所以卤族元素At的单质为有色固体,AgAt可能不溶于水也不溶于稀硝酸,故B正确;
C.元素的金属性越强,其单质与水或酸反应越剧烈,金属性Na>Li,所以Na与水反应比Li与水反应剧烈,故C错误;
D.元素的非金属性越强,其氢化物的稳定性越强,非金属性Se<S,所以氢化物的稳定性,则H2S是比H2Se稳定的气体,故D错误;
故选B.
点评 本题考查元素周期律,为高频考点,明确同一周期、同一主族元素性质递变规律是解本题关键,知道金属性、非金属性强弱判断方法,题目难度不大.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | c(HCN)>c(CN-) | B. | c(Na+)<c(CN-) | ||
| C. | c(HCN)-c(CN-)=c(OH-) | D. | c(HCN)+c(CN-)=2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH | B. | HOOC-COOH | C. | HO(CH2)2CHO | D. | HO- -COOH -COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

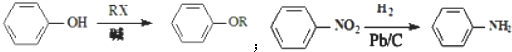

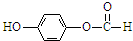 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H3n-12X | B. | H12-3n X | C. | H3n-4X | D. | H4-3nX |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| 甲 | C | 0.2 | pH=7 |
| 乙 | 0.2 | 0.1 | pH=a |
| 丙 | 0.2 | 0.2 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 分子式 | C8H10 | C3H5Cl | C4H8O2 | C4H9ClO |
| 限定条件 | 芳香烃 | 能发生加成反应 | 能与氢氧化钠溶液反应 | 能与钠反应 |
| A. | ③②①④ | B. | ②③①④ | C. | ③①②④ | D. | ②①③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com