
 氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用.
氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用.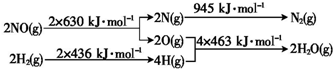
分析 (1)NaH是一种生氢剂属于离子化合物,NaH与H2O反应放出H2.是氢元素发生的归中反应;
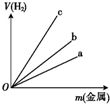
(2)实验室用锌与稀硫酸反应制取H2,发生置换反应生成硫酸锌和氢气,依据氧化还原反应电子守恒分析,同质量的金属,摩尔电子质量越小,生成氢气越多;
(3)储氢过程是气体体积减小的放热反应,结合化学平衡移动原理分析判断需要合适的条件;
(4)根据能量变化图,则反应断键共吸收2×630+2×436=2132kJ,形成共放出945+4×463=2797kJ,所以该反应共放出2797-2132=665kJ的热量,据此书写;
(5)据化学平衡三段式列式计算,
平衡状态c(H2)=c(CH4)=0.8mol/L,c(CO2)=0.2mol/L;
CO2(g)+4H2(g)?CH4(g)+2H2O(g)
起始量(mol/L) 1.0 4.0 0 0
变化量(mol/L) 0.8 3.2 0.8 1.6
平衡量(mol/L) 0.2 0.8 0.8 1.6
①反应速率V=$\frac{△c}{△t}$计算;
②根据平衡常数为生成物浓度的幂次方之积比上反应物浓度的幂次方之积书写;比较300℃与200℃时的平衡常数K的值判断反应的△H;
解答 解:(1)NaH是一种生氢剂属于离子化合物,NaH含有的化学键为离子键,NaH与H2O反应放出H2发生氧化还原反应反应的化学方程式为:NaH+H2O=NaOH+H2↑;
故答案为:离子键,NaH+H2O=NaOH+H2↑;
(2)实验室用锌与稀硫酸反应制取H2,发生置换反应生成硫酸锌和氢气,反应的离子方程式为:Zn+2H+=Zn2++H2↑,依据氧化还原反应电子守恒分析,同质量的金属,摩尔电子质量越小,生成氢气越多,锌、铝、铁分别与稀硫酸反应时金属质量与H2体积的关系可知,同质量的金属生成氢气越多的,其摩尔电子质量越小,摩尔电子质量分别为:Zn为32.5g/mol,Al为9g/mol,Mg为12/mol,所以同质量的金属铝生成氢气最多,图象中c符合;
故答案为:Zn+2H+=Zn2++H2↑,c;
(3)其储氢和放氢的原理可表示为MOFs(s)+nH2(g)$?_{放氢}^{储氢}$(H2)nMOFs(s),△H<0,储氢过程是气体体积减小的放热反应,平衡正向进行,需要的条件为低温高压;
故答案为:B;
(4)根据能量变化图,则反应断键共吸收2×630+2×436=2132kJ,形成共放出945+4×463=2797kJ,所以该反应共放出2797-2132=665kJ的热量,热化学方程式为:2NO(g)+2H2(g)=N2(g)+2H2O(g)△H=-665kJ•moL-1;
故答案为:2NO(g)+2H2(g)=N2(g)+2H2O(g)△H=-665kJ•moL-1;
(5)平衡状态c(H2)=c(CH4)=0.8mol/L,c(CO2)=0.2mol/L;
CO2(g)+4H2(g)?CH4(g)+2H2O(g)
起始量(mol/L) 1.0 4.0 0 0
变化量(mol/L) 0.8 3.2 0.8 1.6
平衡量(mol/L) 0.2 0.8 0.8 1.6
①0~10min内v(H2)=$\frac{3.2mol/L}{10min}$=0.32mol/L•min;
故答案为:0.32mol/L•min;
②反应的平衡常数表达式K=$\frac{c({H}_{2}O){c}^{2}(C{H}_{4})}{c(C{O}_{2}){c}^{4}({H}_{2})}$=$\frac{1.{6}^{2}×0.8}{0.2×0.{8}^{4}}$=25,因为200℃时该反应的平衡常数K=64.8,所以升温K变小,平衡向逆反应方向移动,所以△H<0;
故答案为:25,<.
点评 本题考查了热化学方程式定量计算,化学方程式三段式计算应用,氧化还原反应的理解应用,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖的酯化反应若用浓硫酸作催化剂会炭化发黑:C6H12O6(葡萄糖)$\stackrel{浓硫酸}{→}$ 6C+6H2O | |
| B. | 向AgNO3溶液中加入过量Na2S溶液后,再加入NaCl溶液,黑色沉淀变成白色:Ag2S+2Cl-=2AgCl↓+S2- | |
| C. | 将NH3通入滴有酚酞的水中,溶液变红:NH3+H2O?NH3•H2O?NH${\;}_{4}^{+}$+OH- | |
| D. | 明矾的水溶液pH<7:Al3++3H2O?Al(OH)3(胶体)+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
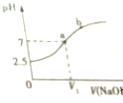 常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )
常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )| A. | NaHSO3溶液呈酸性 | B. | V1<10mL | ||
| C. | 在a点,c(Na+)=c(SO32- )+c(HSO3-) | D. | HSO3-的电离常数Ka=6.25×10-7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
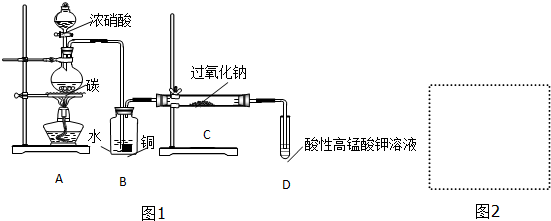
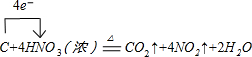 .
.| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,2.24 L苯含有的分子数为0.1NA | |
| B. | 100ml 1mol/L的NH4Cl溶液中,NH4+的数目为0.1NA | |
| C. | 7.8 g Na2S和Na2O2的混合物中所含离子数为0.3NA | |
| D. | 电解精炼铜时,阳极质量每减少32 g,电路中就转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘-131原子核外有5个电子层 | |
| B. | 碘-131原子的最外层有7个电子 | |
| C. | 具有放射性的碘-131原子比普通碘-127原子多4个中子 | |
| D. | 131I2与127I2互为同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com