
����Ŀ����ѧ��Ӧ�Ŀ������ȶ�����������������Ҫ�����塣
��1����Ӱ�췴Ӧ�����������ڿո�
ʵ �� | Ӱ������ |
�� ʳ����ڱ��������ӳ������� | ��__________ |
�� ʵ���ҽ���״ҩƷ��ϸ���ٽ��з�Ӧ | ��__________ |
�� ��H2O2�ֽ���O2ʱ������MnO2 | ��__________ |
�� ʵ�����Ʊ�H2ʱ���ý�Ũ��������Zn����Ӧ | ��__________ |
��2����ͼ��ʾ��800��ʱA��B��C�����������ܱ������з�Ӧʱ��Ũ�ȱ仯������ͼ�ش����⣺
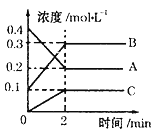
�ٸ÷�Ӧ��������_______________��
��2min�ڣ�C�ķ�Ӧ����Ϊ____________________��
�۸÷�Ӧ�ķ���ʽΪ__________________________��
�������������£����A�ķ�Ӧ����Ϊ0.05mol/(L��s)����ʱ�ķ�Ӧ��800��ʱ��ȣ�______________��
A����800��ʱ�� B����800��ʱ�� C����800��ʱ����һ��
���𰸡��¶� �������� ���� Ũ�� B�� C 0.05 mol /��L��min�� 2A![]() 2B+C B
2B+C B
��������
��1��Ӱ�컯ѧ��Ӧ���ʵ��������¶ȡ�Ũ�ȡ������Լ�����ı������С�ȣ���ʵ���Ŀ�Ŀ���ѡ��Ĵ�ʩ��
��2����ͼ���֪��A�����ʵ���Ũ�ȼ�С��B��C�����ʵ���Ũ�����ӣ���AΪ��Ӧ�B��CΪ������ɷ�Ӧ��Ũ�ȵı仯֮�ȵ��ڻ�ѧ������֮�ȿɵã���c��A������c��B������c��C��=0.2mol/L��0.2mol/L��0.1mol/L=2��2��1����Ӧ�Ļ�ѧ����ʽΪ2A![]() 2B+C��������=
2B+C��������=![]() ���㷴Ӧ���ʣ�
���㷴Ӧ���ʣ�
��1���ٱ������¶Ƚϵͣ������¶ȣ���Ӧ���ʼ�С�����ӳ������ڣ�
�𰸣��¶ȣ�
�ڹ��������Ĵ�СӰ�컯ѧ��Ӧ���ʣ������Խ��Ӧ����Խ�죬ʵ���ҽ���״ҩƷ��ϸ���ɼӿ췴Ӧ���ʣ�
�𰸣�����������
�۴����ܼӿ췴Ӧ���ʣ���H2O2�ֽ���O2ʱ������MnO2�����������ã��ܽϿ��������壻
�𰸣�������
�ܶ�����Һ�еĻ�ѧ��Ӧ������Ӧ��Ũ���ܼӿ췴Ӧ���ʣ��ý�Ũ��������Zn����Ӧ�������������������ʣ���Ũ�Ȳ��ܹ�������Ũ������������������
�𰸣�Ũ�ȣ�
��2������ͼ���֪��A�����ʵ���Ũ�ȼ�С��B��C�����ʵ���Ũ�����ӣ���AΪ��Ӧ�B��CΪ�����
�𰸣�B��C
����(C)=![]() =
=![]() =0.05mol/��Lmin����
=0.05mol/��Lmin����
�𰸣�0.05mol/��Lmin��
���ɷ�Ӧ��Ũ�ȵı仯֮�ȵ��ڻ�ѧ������֮�ȿɵã���c��A������c��B������c��C��=0.2mol/L��0.2mol/L��0.1mol/L=2��2��1����Ӧ�Ļ�ѧ����ʽΪ2A![]() 2B+C��
2B+C��
�𰸣�2A2B+C��
�ܵ�A�ķ�Ӧ����Ϊ0.05mol/��Ls��������C��ʾ������Ϊ������C��=0.025mol/��Ls��=1.5 mol/��Lmin�������ݢڵĽ���ԣ�C��=0.05mol/��Lmin������ʱ�ķ�Ӧ��800��ʱ��ȣ���800��ʱ�죻
�𰸣�B



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ϸ���л�ѧԪ�ص���������ȷ����
A. ϸ����һ��Ԫ�ص������ܱ�����Ԫ�����
B. ϸ���е��������ʶ�����̼Ԫ��
C. ϸ��Ĥ�ϵ���������������ά��ϸ����Ԫ����ɵ�����ȶ�
D. ϸ���е���Ԫ���������ٶ��������Ԫ����Ҫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¶Ȳ���������£��ں��ݵ������н������з�Ӧ��N2O4��g���T2NO2��g������N2O4��Ũ����0.1molL��1����0.07molL��1��Ҫ15s����ôN2O4��Ũ����0.07molL��1����0.05molL��1����ķ�Ӧʱ�䣨 ��
A. ����5s B. ����10s C. ��10s D. ����10s
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������������Һ�к���Mg2����K����Ca2����Fe3������Ũ�ȶ���0.1 mol��L��1������һ��ʱ�������Һ��ʣ��������(����)
A. Fe3�� B. Mg2�� C. K�� D. Ca2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ҫ���л��
CH2=CH2 

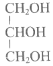
�� �� �� ��
��1��������Һ��ȼ�ϵ���________������ţ���ͬ����
��2�����������ƻ�ױƷ��ʪ�ɷֵ���________��
��3���������Ʊ���ȩ��֬����________��
��4�����������Ϊ����ʯ�ͻ�����չˮƽ�ı�־����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��EΪԭ��������������Ķ�����Ԫ�أ���֪A��B��E 3��ԭ������㹲��11�����ӣ�����3��Ԫ�ص�����������ˮ�����������ܷ�����Ӧ�����κ�ˮ��CԪ�ص������������ȴ�����������4��DԪ��ԭ�Ӵ�����������������������3��
��1��д������Ԫ�ط��ţ�A _______ ��B________��C________��D________��E__________
��2��A��E��Ԫ�ؿ��γɻ�����õ���ʽ��ʾ�仯������γɹ��̣�____________ ��
��3��д��A��B��Ԫ������������ˮ�������Ӧ�Ļ�ѧ����ʽ��______________ ��
��4���Ƚ�C��D������������ˮ��������ԣ����û�ѧʽ��ʾ��_______________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ����
A. 64g SO2�к��е�ԭ����Ϊ3NA
B. 5.6g��������Ϊ����ʱʧȥ�ĵ�����Ϊ0. 3NA
C. ���³�ѹ��,11.2L Cl2���еķ�����Ϊ0.5NA
D. 1mol/L NaOH��Һ��Na+����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��ܴٽ�ˮ�ĵ�������Һ��c(H+)>c(OH-)����
A. NaHSO4 B. CH3COONa C. HCl D. CuSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����(Ru)����������Ⱦ������̫���ܵ�صĹ���ԭ��������з�������Ҫ��Ӧ��ͼ��ʾ������˵���������

A. ��ع���ʱ������ת��Ϊ���ܣ�XΪ��صĸ���
B. �Ʋ����粣���Ϸ���������Ӧ����I-
C. �������Һ�з�����Ӧ:2Ru3++3I-![]() 2Ru2++I3-
2Ru2++I3-
D. ��ع���ʱ���������Һ��I-��I3-��Ũ�Ȼ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com