

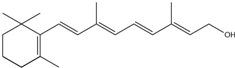
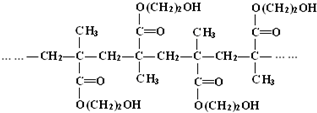
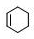
 ,A与溴水发生加成反应生成B为
,A与溴水发生加成反应生成B为 ,B在NaOH/醇条件下发生消去反应生成1,3-环己二烯,反应⑤发生为1,4-加成反应,反应⑥为碳碳双键与氢气发生加成反应生成C为
,B在NaOH/醇条件下发生消去反应生成1,3-环己二烯,反应⑤发生为1,4-加成反应,反应⑥为碳碳双键与氢气发生加成反应生成C为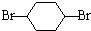 ,C在NaOH水溶液、加热条件下发生水解反应生成D为
,C在NaOH水溶液、加热条件下发生水解反应生成D为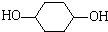 ,反应⑧为醇与乙酸的酯化反应;
,反应⑧为醇与乙酸的酯化反应; ,A与溴水发生加成反应生成B为
,A与溴水发生加成反应生成B为 ,B在NaOH/醇条件下发生消去反应生成1,3-环己二烯,反应⑤发生为1,4-加成反应,反应⑥为碳碳双键与氢气发生加成反应生成C为
,B在NaOH/醇条件下发生消去反应生成1,3-环己二烯,反应⑤发生为1,4-加成反应,反应⑥为碳碳双键与氢气发生加成反应生成C为 ,C在NaOH水溶液、加热条件下发生水解反应生成D为
,C在NaOH水溶液、加热条件下发生水解反应生成D为 ,反应⑧为醇与乙酸的酯化反应,根据上面的分析可知,步骤(4)的反应类型 消去反应,D的结构简式为
,反应⑧为醇与乙酸的酯化反应,根据上面的分析可知,步骤(4)的反应类型 消去反应,D的结构简式为 ,生成A的化学方程式为
,生成A的化学方程式为 ,
, ;
; ;
; 与
与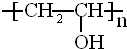 ,
, 与
与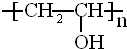 ;
;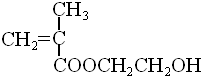 ,单体的名称是甲基丙烯酸乙二醇酯,
,单体的名称是甲基丙烯酸乙二醇酯,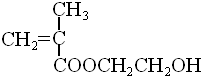 ;甲基丙烯酸乙二醇酯.
;甲基丙烯酸乙二醇酯.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
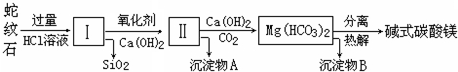
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
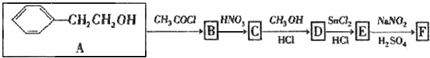
| HCl |

查看答案和解析>>
科目:高中化学 来源: 题型:
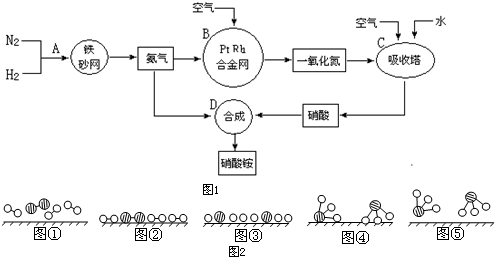
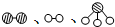 分别表示N2、H2、NH3.
分别表示N2、H2、NH3.
| ||
| △ |
| 注意事项 | 理由 | |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:
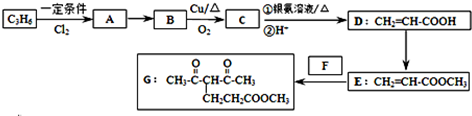
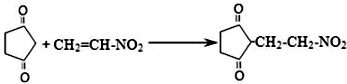
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢管与电源正极连接,可对钢管进行电化学保护 |
| B、利用高压氧舱治疗煤气中毒是依据平衡移动原理 |
| C、配制氯化亚锡(SnCl2)溶液时需加适量盐酸防止被氧化变浑浊 |
| D、用Fe除去溶液中的Cu2+、Hg2+与用FeS除去溶液中的Cu2+、Hg2+的原理相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com