
| A. | 元素Y的最高正化合价为+6 | |
| B. | 离子半径的大小顺序为W>Q>Z>X>Y | |
| C. | 常温下,1molQ单质和足量的NaOH溶液反应转移1mol电子 | |
| D. | 元素W的最高价氧化物对应的水化物酸性比Q的强 |
分析 短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,则Y的氢化物作溶剂,且为氢化物,则Y的氢化物是H2O,所以Y是O元素,X的氢化物能溶于水,且X的原子序数小于Y,所以X是N元素;常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液,铝、铁能溶于稀硫酸却不溶于浓硫酸,Z是短周期主族元素,所以Z是Al,W是S元素,Q属于短周期主族元素且原子序数大于S,所以Q是Cl元素,结合元素周期律来分析解答.
解答 解:由以上分析可知X为N、Y为O、Z为Al、W为S、Q为Cl元素.
A.Y为氧元素,无正价,故A错误;
B.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->Cl->N3->O2->Al3+,即离子半径W>Q>X>Y>Z,故B错误;
C.氯气与氢氧化钠反应生成NaCl、NaClO,Cl元素化合价由0价分别变为-1、+1价,则转移1mol电子,故C正确;
D.非金属性Cl>S,故Cl元素最高价氧化物对应水化物的酸性更强,故D错误,
故选C.
点评 本题考查了原子结构和元素周期律的关系,为高频考点,侧重考查学生的分析能力,题目难度中等,正确推断元素是解本题关键,结合元素周期律来分析解答即可,注意离子半径大小的比较方法,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 加入少量NaOH固体 | B. | 加热升温10℃ | ||
| C. | 加入锌粉 | D. | 加入固体CH3COONa |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 甲烷(乙烯) | 酸性KMnO4溶液 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | 苯(甲苯) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | 溴水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
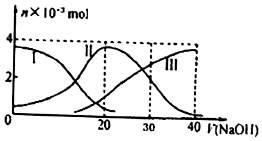
| A. | H2A在水中的电离方程式是:H2A═H++HA-、HA-?H++A2- | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 | |
| C. | 当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+ )+c(HA- )+2c(H2A)═c(A2- )+2c(OH-) | |
| D. | 当V(NaOH)=20 mL时,溶液中各粒子浓度的大小顺序为c(Na+)>c(HA-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
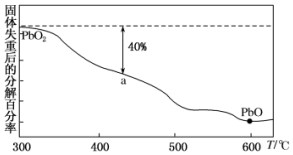 已知铅元素有+2价、+4价两种常用价态,铅及其化合物可用于耐酸设备及X射线防护等.
已知铅元素有+2价、+4价两种常用价态,铅及其化合物可用于耐酸设备及X射线防护等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
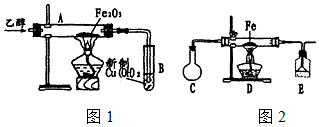
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 医用消毒酒精中乙醇的浓度为95% | |
| B. | 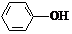 和 和 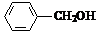 互为同系物 互为同系物 | |
| C. | 常温下,甲醛和乙醛都是无色有刺激性气味的液体 | |
| D. | 苯酚能与碳酸钠溶液反应,但不会产生CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com