
| A. | 流出溶液的体积为(m-n)mL | B. | 流出溶液的体积为(n-m)mL | ||
| C. | 管内溶液体积等于(a-n)mL | D. | 管内溶液体积多于nmL |
分析 滴定管的“0”刻度在上端,满刻度在下端,滴定管刻度值从上到下刻度逐渐增大,滴定管满刻度以下还有一段空间没有刻度,据此即可解答.
解答 解:A.滴定管刻度值从上到下刻度逐渐增大,流出的液体的体积是(n-m)mL,故A错误;
B.滴定管刻度值从上到下刻度逐渐增大,流出的液体的体积是(n-m)mL,故B正确;
C.滴定管的“0”刻度在上端,满刻度在下端,滴定管刻度值从上到下刻度逐渐增大,滴定管满刻度以下还有一段空间没有刻度,AmL滴定管中实际盛放液体的体积大于amL,因此,一支AmL酸式滴定管中盛盐酸,液面恰好在nmL刻度处,把管内液体全部放出,还有满刻度以下的溶液一并放出,总量超过(a-n)mL,故C错误;
D.滴定管的“0”刻度在上端,满刻度在下端,滴定管刻度值从上到下刻度逐渐增大,滴定管满刻度以下还有一段空间没有刻度,amL滴定管中实际盛放液体的体积大于amL,因此,一支amL酸式滴定管中盛盐酸,液面恰好在nmL刻度处,把管内液体全部放出,还有满刻度以下的溶液一并放出,总量超过(a-n)mL,故D错误.
故选B.
点评 本题考查了酸式滴定管的结构,注意滴定管的“0”刻度在上端,满刻度在下端,滴定管满刻度以下还有一段空间没有刻度,是解答的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
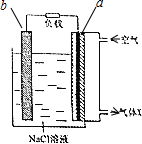 镁-空气电池的工作原理如图所示.下列说法不正确的是( )
镁-空气电池的工作原理如图所示.下列说法不正确的是( )| A. | 工作一段时间后,c(Na+)变大 | B. | 气体X中N2的百分量与空气相同 | ||
| C. | 电池工作时,OH-向a极移动 | D. | 电池总反应为2Mg+O2+2H2O═2Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
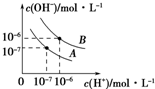 已知水在25℃和95℃时,其电离平衡曲线如图所示.
已知水在25℃和95℃时,其电离平衡曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,溶液中c(OH-)降低 | B. | 加入少量NaOH固体,c(CO32-)增大 | ||
| C. | c(Na+)═2c(CO32-)+c(HCO3-)+c(H2CO3) | D. | c(Na+)+c(H+)═2c(CO32-)+2c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当x=2时,每生成lmolN2,转移电子数为4mol | |
| B. | 该反应中化合价变化的有N和C元素 | |
| C. | 等物质的量N2和C02中,共用电子对的个数比为3:4 | |
| D. | 氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
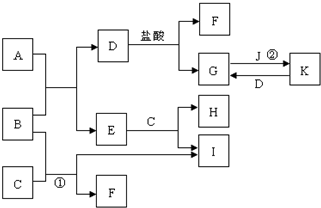 如图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去. A俗称“铁红”,B、D都是日常生活中常见的金属,且B元素是地壳中含量最多的金属元素,常温下,J为黄绿色气体,H为无色气体;C是一种碱,且其焰色反应时,透过蓝色钴玻璃可观察到紫色火焰.
如图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去. A俗称“铁红”,B、D都是日常生活中常见的金属,且B元素是地壳中含量最多的金属元素,常温下,J为黄绿色气体,H为无色气体;C是一种碱,且其焰色反应时,透过蓝色钴玻璃可观察到紫色火焰. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子数 | B. | 分子数 | C. | 质量 | D. | 密度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O已知反应II的产物X的溶液中硫元素的主要存在形式为S2O32-,则II中主要反应的离子方程式为2S2-+5H2O=S2O32-+4H2↑+2OH-.
.反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O已知反应II的产物X的溶液中硫元素的主要存在形式为S2O32-,则II中主要反应的离子方程式为2S2-+5H2O=S2O32-+4H2↑+2OH-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com