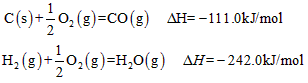“西气东输”工程使北京用上了更加清洁的能源--天然气(主要成分是CH
4)。在使用天然气以前北京用的煤气主要是将碳与水蒸气在高温下反应制得的水煤气,水煤气的主要成分是CO和H
2,两者的体积比约为
1:1。 已知:CO的燃烧热△H=-283.0 kJ/mol;H
2的燃烧热△H=-286.0 kJ/mol;CH
4的燃烧热△H=-890.0 kJ/mol。
(1)用H
2为原料设计成氢氧燃料电池(电解质溶液为KOH),正极的电极反应式是:_______________。
(2)已知:
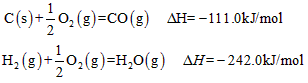
写出由C(s)与H
2O(g)反应生成水煤气的热化学方程式:______________________。
(3)忽略水煤气中其它成分,若获得相等的热量,所需相同状况下水煤气与甲烷的体积比约为_______;排放的CO
2物质的量的比约为_________。通过计算得知:使用天然气能______(填“增多”或“减少”)温室气体(CO
2)的排放。(各种燃料均完全燃烧)
(4)若将由amolCH
4、CO和H
2组成的混合气体完全燃烧,生成CO
2气体和液态水时放出热量(Q)的取值范围是___________。