
| X | Y | ||
| Z | W |
| A. | 钠与Y只能形成Na2Y | |
| B. | Z形成的单质易溶于由X与Z形成的化合物 | |
| C. | Z得电子能力比W强 | |
| D. | X有多种同素异形体,而Y不存在同素异形体 |
分析 由短周期元素X、Y、Z、W在元素周期表中的位置可知,X、Y处于第二周期,Z、W处于第三周期,X元素的原子内层电子数是最外层电子数的一半,则最外层电子数为4,故X为碳元素,则Y为O元素、Z为S元素、W为Cl元素,据此解答.
解答 解:由短周期元素X、Y、Z、W在元素周期表中的位置可知,X、Y处于第二周期,Z、W处于第三周期,X元素的原子内层电子数是最外层电子数的一半,则最外层电子数为4,故X为碳元素,则Y为O元素、Z为S元素、W为Cl元素.
A.Na和O可形成Na2O、Na2O2 ,故A错误;
B.X与Z形成的化合物为二硫化碳,硫单质易溶于二硫化碳,故B正确;
C.同周期自左而右非金属性增强,得电子能力增强,故S得电子能力比Cl弱,故C错误;
D.碳元素有金刚石、石墨、C60等多种同素异形体,氧元素存在氧气、臭氧同素异形体,故D错误;
故选B.
点评 本题考查结构性质位置关系,难度中等,注意整体把握元素周期表的结构,有利于基础知识的巩固.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
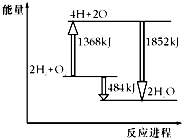 如图为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图,下列说法不正确的是( )
如图为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图,下列说法不正确的是( )| A. | 拆开2molH2(g)和1molO2(g)中的化学键成为H、O原子,共吸收1368kJ能量 | |
| B. | 由H、O原子形成2molH2O(g),共放出1852kJ能量 | |
| C. | 2molH2(g)和1molO2(g)反应生成2molH2O(g),共吸收484kJ能量 | |
| D. | 2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
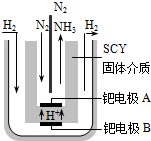 合成氨工业及硝酸工业对工、农生产和国防都有重要意义.请回答:
合成氨工业及硝酸工业对工、农生产和国防都有重要意义.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
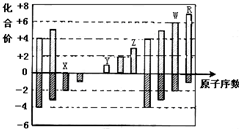
| A. | WX3和水反应形成的化合物是弱电解质 | |
| B. | 气态氢化物的还原性:R>W | |
| C. | 离子半径:Z>Y>X | |
| D. | Y、Z、R三种元素分别形成的最高价氧化物对应的水化物两两间能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量数为198 | B. | 中子数为140 | C. | 质子数为82 | D. | 核外电子数为58 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
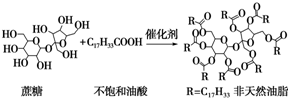
| A. | 蔗糖酯属于油脂类物质 | |
| B. | 该非天然油脂为高分子化合物 | |
| C. | 该非天然油脂与氢氧化钠溶液共热,其水解产物不与溴水反应 | |
| D. | 该蔗糖酯在稀硫酸的作用下水解,最终可生成三种有机化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
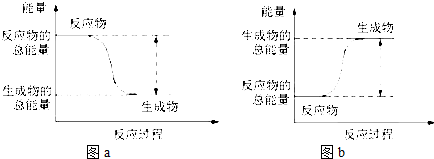
| A. | 图a表示的是吸热反应的能量变化 | |
| B. | 图b中反应物比生成物稳定 | |
| C. | 图b可以表示氯化铵固体与氢氧化钡晶体反应的能量变化 | |
| D. | 图a不需要加热就一定能发生,图b一定需要加热才能发生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com