
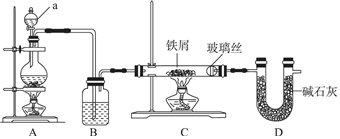
·ÖĪö ÓÉĢāøųŠÅĻ¢æÉÖŖ£¬×°ÖĆAŹĒÖʱøĀČĘųµÄ·¢Éś×°ÖĆ£¬Éś³ÉµÄĀČĘųÖŠŗ¬ĀČ»ÆĒāŗĶĖ®ÕōĘų£¬Ķعż×°ÖĆBÖŠÅØĮņĖįøÉŌļĀČĘų£¬Ķعż×°ÖĆC·“Ӧɜ³ÉĪŽĖ®ĀČ»ÆĢś£¬Ź£ÓąĘųĢåĶعżD×°ÖĆÖŠµÄ¼īŹÆ»ŅĪüŹÕ£¬²¢ĶعżD×°ÖĆĪüŹÕæÕĘųÖŠµÄĖ®ÕōĘų£¬·ĄÖ¹¶ŌĀČ»ÆĢśÖʱøµÄøÉČÅ£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗ£Ø1£©ÓÉŅĒĘ÷¹¹ŌģæÉÖŖaĪŖ·ÖŅŗĀ©¶·£¬A×°ÖĆÖĘČ”µÄŹĒĀČĘų£¬ŹµŃéŹŅ³£ÓĆÅØŃĪĖįÓė¶žŃõ»ÆĆĢ¼ÓČČÖĘČ”£¬»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗMnO2+4HCI£ØÅØ£© $\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£¬B×°ÖĆŹ¢·ÅÅØĮņĖįøÉŌļĀČĘų£»
¹Ź“š°øĪŖ£ŗ·ÖŅŗĀ©¶·£»MnO2+4HCI£ØÅØ£© $\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£»ÅØĮņĖį£»
£Ø2£©ŹµŃéÖŠÓŠĀČĘųÉś³É£¬ĖłŅŌŅŖĻČ¼ģŃ鏵Ńé×°ÖƵÄĘųĆÜŠŌ£¬ĪŖÅųż×°ÖĆÖŠµÄæÕĘų£¬Ó¦ĻȵćČ¼A“¦µÄ¾Ę¾«µĘ£¬Éś³ÉĀČĘųÅųżæÕĘųÖŠµÄŃõĘųŗĶĖ®ÕōĘų£¬CÖŠ³äĀś»ĘĀĢÉ«ĘųĢåŗó£¬ŌŁµćČ¼C“¦¾Ę¾«µĘ£»
¹Ź“š°øĪŖ£ŗ¼ģ²é×°ÖĆĘųĆÜŠŌ£»A£»CÖŠ³äĀś»ĘĀĢÉ«ĘųĢ壻C£»
£Ø3£©×°ÖĆDÖŠ¼īŹÆ»ŅµÄ×÷ÓĆŹĒ³żČ„Ī“·“Ó¦µÄĀČĘų ·ĄÖ¹æÕĘųÖŠµÄĖ®ÕōĘų½ųČėC×°ÖĆ£»
¹Ź“š°øĪŖ£ŗ³żČ„Ī“·“Ó¦µÄĀČĘų£»·ĄÖ¹æÕĘųÖŠµÄĖ®ÕōĘų½ųČėC×°ÖĆ£»
£Ø4£©³żČ„ĀČĘųÖŠµÄĀČ»ÆĒāĘųĢåÓƱ„ŗĶŹ³ŃĪĖ®£¬Ö»ŅŖĀČĘų×ćĮ棬×īÖÕ²śĪļÖ»ÓŠĀČ»ÆĢś£¬²»ŠčŅŖ³żČ„ĀČ»ÆĒā£»
¹Ź“š°øĪŖ£ŗ±„ŗĶŹ³ŃĪĖ®£»Ö»ŅŖĀČĘų×ćĮ棬×īÖÕ²śĪļÖ»ÓŠĀČ»ÆĢś£®
µćĘĄ ±¾ĢāŅŌĀČ»ÆĢśŅŌ¼°ĀČ»ÆŃĒĢśµÄÖĘČ”ĪŖŌŲĢ壬漲éµÄŹĒŹµŃéŹŅÖŠĀČĘųµÄÖĘČ”·½·Ø”¢³£¼ūĪ²ĘųµÄ“¦Ąķ·½·Ø£¬Ć÷Č·ĀČĘųÖʱøŌĄķŗĶŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | Y”¢QĮ½ÖÖŌŖĖŲµÄĘųĢ¬Ēā»ÆĪļ¼°Ęä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ¾łĪŖĒæĖį | |
| B£® | ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄ¼īŠŌ£ŗZ£¼M | |
| C£® | ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗR£¾Q | |
| D£® | ¼ņµ„Ąė×ӵİė¾¶£ŗX£¾Z£¾M |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 ŹµŃéŹŅŠčŅŖÅäÖĘ100mL 0.1mol•L-1 CuSO4ČÜŅŗ£®
ŹµŃéŹŅŠčŅŖÅäÖĘ100mL 0.1mol•L-1 CuSO4ČÜŅŗ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ĪļÖŹ | FeS | MnS | HgS |
| ČܶȻż | 5.0”Įl0-18 | 4.6”Įl0-14 | 2.2”Įl0-54 |
| ³ĮµķĪļ | Fe£ØOH£©3 | Fe£ØOH£©2 | Mn£ØOH£©2 |
| æŖŹ¼³ĮµķµÄpH | 2.7 | 7.6 | 8.3 |
| ĶźČ«³ĮµķµÄpH | 3.7 | 9.7 | 9.8 |
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”÷H1£¾”÷H2£»”÷H3£¼”÷H4 | B£® | ”÷H1£¾”÷H2£»”÷H3£¾”÷H4 | C£® | ”÷H1=”÷H2£»”÷H3£¼”÷H4 | D£® | ”÷H1£¼”÷H2£»”÷H3£¾”÷H4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹ā»ÆѧŃĢĪķÓė“óĮæÅÅ·ÅĢ¼Ēā»ÆŗĻĪļŗĶµŖŃõ»ÆŗĻĪļÓŠ¹Ų | |
| B£® | ĪŖ·ĄÖ¹³ōŃõæÕ¶“µÄĄ©“ó£¬ĮŖŗĻ¹ś»·±£×éÖÆŅŖĒóø÷¹ś“óĮæ¼õÉŁCO2µÄ¹¤ŅµÅÅ·ÅĮæ | |
| C£® | ĆŽ»Ø”¢²ĻĖæŗĶ½õĀŚµÄÖ÷ŅŖ³É·Ö¶¼ŹĒĻĖĪ¬ĖŲ | |
| D£® | ĪŖĮĖ·ĄÖ¹ÖŠĒļŌĀ±żµČø»ŗ¬Ö¬Ź³Ę·Ńõ»Æ±äÖŹ£¬ŃÓ³¤±£ÖŹĘŚ£¬æÉŅŌ°ü×°“üÖŠ·ÅČėÉśŹÆ»Ņ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com