
【题目】下列图示与对应的叙述相符的是( )

A.图1曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,P点时二者恰好反应完全且溶液呈中性
B.图2表示![]() 与
与![]() 反应生成
反应生成![]() 或
或![]() 时的能量变化的关系
时的能量变化的关系
C.图3表示向![]() 溶液中滴入NaOH溶液时所得沉淀质量的变化
溶液中滴入NaOH溶液时所得沉淀质量的变化
D.由图4表示的反应速率随温度变化的关系可知该反应的![]()
【答案】A
【解析】
A. 分析图象可知,P点为突变点,此时二者恰好反应完全;
B. H2(g)与O2(g)反应生成H2O(l)放出能量多,生成H2O(g)放出热量少;
C. 向Ba(HCO3)2溶液中滴入NaOH溶液,反应开始即有沉淀生成;
D. 由图可知,升高温度逆反应速率比正反应速率增大快。
A. 由图象可知,盐酸与氢氧化钠浓度都是![]() ,P点为突变点,此时二者恰好反应完全,生成的NaCl显中性,与图象相符,故A正确;
,P点为突变点,此时二者恰好反应完全,生成的NaCl显中性,与图象相符,故A正确;
B. 液化放热,所以能量H2O(g)> H2O(l), 产物能量越高,反应放热越少,所以H2(g)与O2(g)反应生成H2O(l)放出能量更多,与图象不符,故B错误;
C. 向Ba(HCO3)2溶液中滴入NaOH溶液,OH-和HCO3-反应生成CO32-立即和Ba2+反应生成BaCO3沉淀,所以,反应开始即有沉淀生成,图象中沉淀生成不是从0点开始的,故C错误;
D. 升高温度,逆反应速率比正反应速率增大快,图形交点处达到平衡,继续升高温度,v(逆)> v(正),平衡向逆反应方向移动,所以,正反应方向为放热反应,![]() ,故D错误;
,故D错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】某硫酸镁和硫酸铝的混合溶液中,c(Mg2+ )=2 mol·L-1,c(SO42-)=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+分离,至少应加入1.6 mol·L-1氢氧化钠溶液的体积是
A.0.5 L B.1.625 LC.1.8 LD.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,物质的量之比为2∶1的SO2和O2的混合气体在容积为2 L的恒容密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g)(正反应为放热反应),n(SO2)随时间变化关系如下表:
2SO3(g)(正反应为放热反应),n(SO2)随时间变化关系如下表:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
下列说法正确的是( )
A. 当容器中气体的密度不变时,该反应达到平衡状态
B. 该反应进行到第3分钟时,逆反应速率小于正反应速率
C. 从反应开始到达到平衡,用SO3表示的平均反应速率为0.01 mol/(L·min)
D. 容器内达到平衡状态时的压强与起始时的压强之比为5∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正四面体烷是一种可能存在的柏较图轻,IUPAC名称为三环[1. 1. 0. 0]丁烷。其球棍模型如图所示。下列关于该化合物的说法正确的是

A. 与环丁二烯互为同分异构体
B. 二氯代物超过两种
C. 碳碳键键角为109°28'
D. 三环[1.1. 0.0] 丁烷生成1 mol 丁烷至少需要2mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标号为①~⑩的元素,在元素周期表中的位置如下:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
试回答下列问题:
(1)(填写元素符号)① _____③______⑤_____ ⑦_____
(2)①和④号元素形成的化合物的化学式________,用电子式表示其形成过程为__________。
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是: ______﹥_________ (填化学式)。⑨和⑩号元素的最高价氧化物的水化物的酸性是: ______ ﹥_________ (填化学式)。
(4)①、⑤、⑦号元素形成的一种化合物的电子式是________,在该化合物中既含有________键,又含有________键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定乙醇的结构式,有人设计了用无水酒精与钠反应的实验装置和测定氢气体积的装置进行实验。可供选用的实验仪器如图所示。
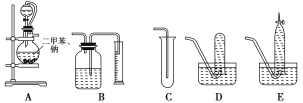
请回答以下问题:
(1)测量氢气体积的正确装置是________(填写编号)。
(2)装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是________(填写编号)。
A.防止无水酒精挥发
B.保证实验装置不漏气
C.使无水酒精容易滴下
(3)实验前预先将小块钠在二甲苯中熔化成小钠珠,冷却后倒入烧瓶中,其目的是
________________________________________________________________________。
(4)已知无水酒精的密度为0.789 g·cm-3,移取2.0 mL酒精,反应完全后(钠过量),收集390 mL气体。则乙醇分子中能被钠取代出的氢原子数为________,由此可确定乙醇的结构式为________________而不是____________________________________________________。
(5)实验所测定的结果偏高,可能引起的原因是________(填写编号)。
A.本实验在室温下进行
B.无水酒精中混有微量甲醇
C.无水酒精与钠的反应不够完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构如图所示,下列说法正确的是

A. 该有机物的分子式为C21H24O4
B. 该有机物共有四种官能团,分别是:羟基、羧基、苯环、碳碳双键
C. 该有机物最多消耗NaOH与NaHCO3的物质的量比为1:1
D. 1mol 该有机物与足量金属钠反应,生成33.6L氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL 18mol/L的硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量
A. 小于0.45mo1B. 等于0.45molC. 在0.45mol和0.9mol之间D. 大于0.9mo1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子和少量的尿素[CO(NH2)2].利用该卤块为原料生产轻质氧化镁的工艺流程如图:

当相关金属离子[c0(Mn+)=0.1molL﹣1]时,形成氢氧化物沉淀的pH范围如表:
金属离子 | Fe2+ | Fe3+ | Mn2+ | Mg2+ |
开始沉淀的pH | 7.6 | 2.7 | 8.3 | 9.6 |
沉淀完全的pH | 8.3 | 3.7 | 9.8 | 11.1 |
回答下列问题:
(1)NaClO中氯元素的化合价为_____。NaClO为漂白液的主要成分,写出制备漂白液的离子方程式_____。
(2)若溶液b中杂质离子的浓度均为0.1molL﹣1,若要使杂质离子沉淀完全,步骤③应溶液的pH调节至_____,沉淀物A含有Mn(OH)2和_____。
(3)若在实验室中完成步骤⑥,则沉淀物C应在_____(填仪器名称)中灼烧。写出步骤⑥的化学方程式_____。
(4)步骤②加入NaClO还能除去卤块中的尿素[CO(NH2)2],生成一种盐和两种无毒气体及水,其化学方程式为_____,若除去卤快中含有的0.02molCO(NH2)2,需消耗NaClO的质量为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com