
| A、用湿润的pH试纸测稀碱液的pH,测定值偏小 |
| B、酸碱中和滴定时用待测液润洗锥形瓶,所测结果偏高 |
| C、滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小 |
| D、测定中和反应的反应热时,将碱缓慢倒入酸中,所测最高温度值偏大 |


科目:高中化学 来源: 题型:
 某同学设计了如图装置(夹持仪器省略)进行系列实验时,将药品A逐滴加入到固体B中,请根据下列实验回答问题.
某同学设计了如图装置(夹持仪器省略)进行系列实验时,将药品A逐滴加入到固体B中,请根据下列实验回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:
 (双烯合成,也可表示为
(双烯合成,也可表示为 )
)

| 2H2 |
| Ni |
| -2H2O |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe在氯气中燃烧生成FeCl2 |
| B、SiO2的化学性质不活泼,不与任何酸发生反应 |
| C、常温下,铝制品用浓硫酸或浓硝酸处理过,可耐腐蚀 |
| D、铁粉中混有铝粉既可用过量的NaOH溶液,也可以用过量FeCl3溶液充分反应过滤除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 表示向1L浓度均为0.1mol.L-1的Ba(OH)2、NaAlO2混合液中逐滴加入0.1mol.L-1稀H2SO4溶液 |
B、 表示常温下,两份足量、等浓度的盐酸与等量锌粉反应时,其中一份滴加了少量硫酸铜溶液 |
C、 表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 |
D、 表示向醋酸溶液中滴入氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
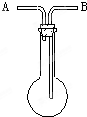 洗气瓶用途的延伸:利用如图所示的装置收集以下8种气体:
洗气瓶用途的延伸:利用如图所示的装置收集以下8种气体:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等浓度的HCN溶液NaCN溶液等体积混合,所得溶液pH>7,则溶液中离子浓度:c(Na+ )>c(CN-)>c(OH- )>c(H+ ) | ||||
| B、0.4mol?L-1某一元酸HA溶液和0.2 mol?L-1NaOH溶液等体积混合的溶液中:2c(OH- )+c(A- )=2c(H+ )+c(HA) | ||||
| C、常温下等浓度的Na2SO3与NaHSO3溶液等体积混合后溶液的pH=7.2,调整比例当溶液呈中性时:c(Na+ )>c(HSO3-)>c(SO32-)>c(H+ )═c(OH- ) | ||||
D、两种弱酸HX和HY混合后,溶液中的c(H+ )为(Ka为电离平衡常数):c(H+ )=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol.L-1氢氯酸(HCN)的pH约为3 |
| B、常温下,pH=4的氢氯酸稀释100倍后所得溶液pH<6 |
| C、10mL 1 mol.L-1氢氯酸(HCN)恰好与10mL 1 mol.L-1NaOH溶液完全反应 |
| D、常温下,0.1mol.L-1NaCN溶液的pH约为10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com