
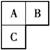
A、B、C短周期元素在周期表中的位置如右图所示,已知A、C可分别与B形成化合物x和y,A与B的质子数之和为C的质子数。现有以下说法,其中判断正确的组合为 ( )
 ①B与C均存在同素异形体
①B与C均存在同素异形体
②x的种类比y的多
③常温下,B的氢化物中无H+
④C的最高价氧化物对应水化物能与A的氢化物形成盐
A.①②③④ B.②④ C.①②④ D.①②
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列对化学反应热问题的说法正确的是( )
A.放热反应发生时不必加热
B.化学反应一定有能量变化
C.一般地说,吸热反应加热后才能发生
D.化学反应的热效应数值与参加反应的物质的多少无关
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。
①A元素最外层电子数是次外层电子数的2倍。
②B的阴离子和C的阳离子与氖原子的电子层结构相同。
③在通常状况下,B的单质是气体,0.1 mol B的气体与足量的氢气完全反应共有0.4 mol电子转移。
④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应生成B的单质。
⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。
请写出:
(1)A元素的最高价氧化物的电子式 。
(2)B元素在周期表中的位置 。
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有 。
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为
。
(5)C与D能形成原子个数比为2∶1的化合物,用电子式表示该化合物的形成过程 。
(6)元素D与元素E相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填选项序号)。
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
查看答案和解析>>
科目:高中化学 来源: 题型:
我国许多城市为了减少燃煤造成的大气污染,对煤做了多方面的改进:
(1)为了除去煤中的含硫化合物,采用FeCl3脱硫,即用FeCl3溶液浸洗煤粉,发生反应如下:FeS2+14FeCl3+8H2O====2FeSO4+13FeCl2+16HCl(已知FeS2中硫元素的化合价为-1价)。
①该反应的氧化剂是 ,若有1 mol FeS2被除去,则发生转移的电子的物质的量是 。
②为了充分利用Fe2+并减少酸(HCl)污染,本方法中可利用工业废铁屑和Cl2让废液重新生成FeCl3。请写出这一过程中有关的离子方程式:
; 。
(2)另一种方法是采用“钙基固硫法”,即在燃煤中加入生石灰,使含硫煤在燃烧时生成的SO2不能逸出而进入炉渣中,试写出表示这一“固硫”过程的化学方程式。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
CO和NO都是汽车尾气里的有害物质,它们能缓慢地起反应生成氮气和二氧化碳:2CO+2NO====N2+2CO2。对此反应下列叙述正确的
是 ( )
A.使用催化剂不改变反应速率
B.改变压强对反应速率没有影响
C.冬天气温低,反应速率降低,对人体危害更大
D.无论外界条件怎样改变,均对此化学反应的速率无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)元素甲是第3周期ⅦA族元素,甲元素与另两种非金属元素可组成离子化合物A。写出A的化学式 ,A中含有的化学键是 。
(2)在第3周期元素的气态氢化物中,元素乙的氢化物最稳定,写出元素乙的单质与水反应的化学方程式 。
(3)金属元素丙形成的某化合物的溶液常用于检验CO2,则元素丙的简单离子与
元素甲的简单离子的半径大小关系是 (用离子符号表示),
元素丁的原子序数比丙小8,写出元素丁的单质在CO2中燃烧的化学方程式
。
(4)元素戊是第3周期中简单离子半径最小的元素,写出该元素的最高价氧化物对应水化物与NaOH溶液反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y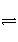
 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
A.33% B.40% C.50% D.65%
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物完全燃烧时只生成水和二氧化碳,且两者的物质的量之比为3∶2,则( )
A.该有机物含碳.氢.氧三种元素 B.该化合物是乙烷
C.该化合物分子中碳.氢原子个数之比是2∶3
D.该有机物含2个碳原子,6个氢原子,但不能确定是否含氧原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com