
| A. | SO2通入溴水中:SO2+2H2O+Br2═2H++SO42-+2HBr | |
| B. | 向漂白粉稀溶液中通入过量CO2:ClO-+CO2+H2O═HClO+HCO3- | |
| C. | NaHSO4溶液和Ba(OH)2溶液充分反应后溶液显中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
分析 A.溴化氢为强酸,应拆成离子形式;
B.二氧化碳过量,反应生成次氯酸和碳酸氢钙;
C.NaHSO4溶液和Ba(OH)2溶液充分反应后溶液显中性则消耗的硫酸氢钠与氢氧化钡物质的量之比为2:1;
D.不符合反应客观事实,三价铁离子能够氧化碘离子.
解答 解:A.SO2通入溴水中,离子方程式:SO2+2H2O+Br2═4H++SO42-+2Br-,故A错误;
B.向漂白粉稀溶液中通入过量CO2,离子方程式:ClO-+CO2+H2O═HClO+HCO3-,故B正确;
C.NaHSO4溶液和Ba(OH)2溶液充分反应后溶液显中性,离子方程式:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C错误;
D.氢氧化铁溶于氢碘酸中的离子反应为2I-+2Fe(OH)3+6H+═2Fe2++6H2O+I2,故D错误;
故选:B.
点评 本题考查离子反应方程式书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、氧化还原反应的离子反应考查,题目难度不大,注意化学式的拆分、注意反应遵循客观事实.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯气以液态形式存在时可称为氯水或液氯 | |
| B. | 红热的铜丝在氯气中燃烧,冒蓝色烟 | |
| C. | 有氯气参加的化学反应必须在溶液中进行 | |
| D. | 钠在氯气中燃烧生成白色固体氯化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯 | B. | 1-丁炔 | ||
| C. | 丁烯 | D. | 2-甲基-1,3-丁二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
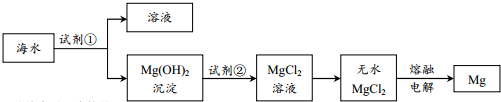
| A. | 为使海水中的MgSO4转化成Mg(OH)2,试剂①可选择石灰乳 | |
| B. | 加入试剂①后,分离得到Mg(OH)2沉淀的方法是过滤 | |
| C. | 加入试剂②反应的离子方程式为:OH-+H+=H2O | |
| D. | 通过电解熔融的无水MgCl2得到48gMg,共转移4mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖在硫酸催化下水解,只生成葡萄糖 | |
| B. | 石油的裂解、煤的干馏都是化学变化 | |
| C. | 1L1mol•L-1AlCl3溶液中含Al3+数目为6.02×1023 | |
| D. | 等质量的铝粉按a、b两种途径完全转化,途径a比途径b消耗更多的NaOH 途径a:Al$→_{点燃}^{O_{2}}$Al2O3$\stackrel{NaOH溶液}{→}$NaAlO2;途径b:Al$\stackrel{NaOH溶液}{→}$NaAlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向0.10mol•L-1NaHSO3溶液中通入NH3至溶液pH=7(通入气体对溶液体积的影响可忽略):c(Na+)>c(SO32-)>c(NH4+) | |
| B. | 0.1mol/L醋酸钠溶液20mL与0.1mol•L-1盐酸10mL混合后的溶液中:c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) | |
| C. | 已知Kw(HF)>Kw(CH3COOH),pH相等的NaF与CH3COOK两溶液中:c(Na+)-c(F-)>c(K+)-c(CH3COO-) | |
| D. | 0.1mol•L-1醋酸溶液和0.2mol•L-1醋酸钠溶液等体积混合后的溶液中:3c(H+)+2c(CH3COOH)=c(CH3COO-)+3c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 反应 温度/℃ | c(H2O2)/ mol•L-1 | V(H2O2) /mL | m(MnO2) /g | t/min |
| 1 | 20 | 2 | 10 | 0 | t1 |
| 2 | 20 | 2 | 10 | 0.1 | t2 |
| 3 | 20 | 4 | 10 | 0.1 | t3 |
| 4 | 40 | 2 | 10 | 0.1 | t4 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 含杂质的物质 | 试剂 | 除杂方法 |
| A | CH4(C2H4) | Br2水 | 洗气 |
| B | C6H6(Br2) | Fe粉 | 蒸馏 |
| C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
| D | C2H2(H2S) | CuSO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com