
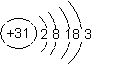
门捷列夫制作元素周期表时,许多元素尚未发现,他在铝的下面留了空位给“类铝”,并对“类铝”的性质进行了预测, “类铝”与后发现的镓的性质一致,从而验证了元素周期表的正确性。下列有关镓的性质的描述中错误的是 ( )
 A.镓的金属性比铝弱 B.镓的常见化合价为+3
A.镓的金属性比铝弱 B.镓的常见化合价为+3
C.镓的原子半径比铝大 D.镓的原子结构示意图为
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如图所示。
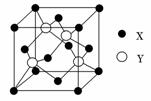
①在1个晶胞中,X离子的数目为________。
②该化合物的化学式为________。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是________。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是________。
(4)Y与Z可形成YZ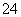 。
。
①YZ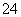 的空间构型为________(用文字描述)。
的空间构型为________(用文字描述)。
②写出一种与YZ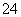 互为等电子体的分子的化学式:________。
互为等电子体的分子的化学式:________。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是
( )
A.3Br2+6KOH====5KBr+KBrO3+3H2O
B.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
C.2KNO3 2KNO2+O2↑
2KNO2+O2↑
D.NH4NO3 N2O↑+2H2O
N2O↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学通过系统实验探究铝及其化合物的性质,操作正确且能达到目的的是 ( )
A.用互相滴加的方法可鉴别氯化铝溶液、氢氧化钠溶液
B.向氯化铝溶液中滴加过量氨水,最终得到澄清溶液
C.常温下铝与浓硝酸反应制得大量的NO2
D.AlCl3溶液加热蒸干得到无水氯化铝晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表是指导化学学习的重要工具。下图为元素周期表的一部分。请按要求填空。

(1)N在元素周期表中的位置是_____;N和F处于同一行,是由于它们的_________相同。
(2)以上元素中,原子半径最小的是_____(写元素符号);最高价氧化物对应水化物中酸性最强的是__________(写化学式)。
(3)Mg和Al中,金属性较强的是_______(写元素符号),写出一条能说明该结论的事实____________________。
(4)S和Cl中,非金属性较强的是_____(写元素符号),不能说明该结论的事实是_____。
a.氯气与铁反应生成FeCl3,硫与铁反应生成FeS
b.把Cl2通入H2S溶液中能发生置换反应
c.受热时H2S易分解,HCl不易分解
d.单质硫是固体,氯的单质是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路。
其化学原理为:2FeCl3 + Cu→ 2FeCl2 + CuCl2。某实验小组的同学对该厂生产印刷电路后所得的废液进行了分析:取50.00 mL 废液,向其中加入足量的AgNO3溶液,析出沉淀43.05g(假设反应前后溶液的体积变化均忽略不计)。试回答:
(1)该厂使用的FeCl3溶液(原的)物质的量浓度________________;
(2)若向250.00 mL废液中加入足量的铜粉,充分反应后,铜粉质量减轻9.6g。
① 充分反应后的溶液中Cu2+的物质的量为 ;
② 原废液中各金属阳离子的物质的量浓度之比为: ;
(书写时须将离子符号和物质的量浓度做一一对应)
查看答案和解析>>
科目:高中化学 来源: 题型:
铝及其化合物用途广泛。工业上焙烧明矾【KAl(SO4)2·12H2O】可得到A12O3,反应的化学方程式为4KAl(SO4)2·12H2O+3S 2K2SO4+2A12O3+9SO2↑+48H2O。
2K2SO4+2A12O3+9SO2↑+48H2O。
请回答下列问题:
(1)在焙烧明矾的反应中,被氧化和被还原的元素质量之比是________________。
(2)焙烧明矾时产生的SO2可用来制硫酸。已知25℃、10lkPa时:

(3)工业上利用电解熔融的A12O3制备Al,其化学方程式是_____________________;电解时阳极和阴极材料均为石墨,电解时所消耗的电极是__________(填“阳极”或“阴极”)。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液,可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式为____________________;
②电池总反应的化学方程式为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在如图所示装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备白色的Fe(OH)2沉淀。

(1)在试管Ⅰ里加入的试剂是____________。
(2)在试管Ⅱ里加入的试剂是____________。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是________________________________________________。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是_______________ __________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com