
【题目】下列说法中不正确的是
A. K2FeO4可代替Cl2处理饮用水,有杀菌消毒作用
B. CaO2属于碱性氧化物,也属于离子化合物,其阴阳离子个数比为1:2
C. 浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了保鲜水果
D. 高温下可用金属钠还原四氯化钛来制取金属钛
科目:高中化学 来源: 题型:
【题目】钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强 合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中 制备金属钼的主要流程图。
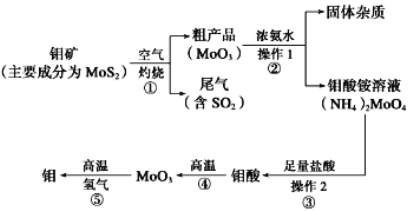
(1)写出在高温下发生反应①的化学方程_________________________________________
(2)生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:______________________________
(3)如果在实验室模拟操作 1 和操作 2,则需要使用的主要玻璃仪器有______________________________
(4)某同学利用下图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:
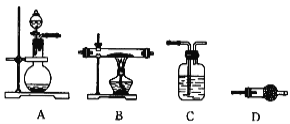
① 请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是______________________________
② 在烧瓶 A 中加入少量硫酸铜的目的是_____
③ 两次使用 D 装置,其中所盛的药品依次是_____、_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重金属离子具有毒性,强碱性溶液不能直接排放到自然界中。实验室中有甲、乙两种废液,甲废液经化验呈碱性,主要有毒离子为Ba2+。如将甲、乙两废液按一定比例混合,毒性明显降低,且可排放到自然界中。则乙废液中可能含有的离子是
A. K+和SO42- B. Cu2+和Cl-
C. Cu2+和SO42- D. Cu2+和CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1.0L密闭容器中放入0.10 molA(g),在一定温度进行如下反应:A(g) ![]() B(g)+C(g)△H=+85.1kJmol-1,反应时间(t)与容器内气体总压强(p)的数据见下表:
B(g)+C(g)△H=+85.1kJmol-1,反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 ______ 。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为 ______,平衡时A的转化率为 ______。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总= ______ mol,n(A)= ______ mol。
②下表为反应物A浓度与反应时间的数据,计算:α= ______。
反应时间t/h | 0 | 4 | 8 | 16 |
c(A)/(molL-1)) | 0.10 | a | 0.026 | 0.0065 |
分析该反应中反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是 ______,由此规律推出反应在12h时反应物的浓度c(A)为 ______ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组依据反应:SO2(g)+Cl2(g)![]() SO2Cl2(g)△H<0,设计制备磺酰氯SO2Cl2的装置如图:
SO2Cl2(g)△H<0,设计制备磺酰氯SO2Cl2的装置如图:

有关信息如表所示:
SO2Cl2 | Cl2 | SO2 | |
熔点/℃ | -54.1 | -101 | -72.4 |
沸点/℃ | 69.1 | -34.6 | -10 |
性质 | 遇水发生剧烈水解 | / | / |
(1)若用浓盐酸与二氧化锰为原料制取Cl2,反应的化学方程式为 ______。
(2)B仪器的作用是 ______。
(3)为了便于混合物的分离且提高反应物的转化率,A装置的反应条件最好选择 ______。
a.冰水浴 b.常温 c.加热至69.1℃
(4)如果通入的Cl2或SO2含有水蒸气,氯气和二氧化硫可能发生反应的化学方程式为 ______ .
(5)实验时先通入干燥的Cl2将A装置中的空气赶走,再缓慢通入干燥的SO2,即发生反应.充分反应后,继续通入Cl2使装置中的SO2进入烧杯中被吸收。分离产物后,向获得的SO2Cl2中加水,出现白雾,振荡、静置得到无色溶液W。
①经分析SO2Cl2与H2O反应属于非氧化还原反应,写出该反应的化学方程式_________________。
②无色溶液W中的阴离子除含少量OH-外,还含有其它两种阴离子,检验溶液W中这两种阴离子方法是______。
③反应完成后,在W溶液、烧杯中分别滴加过量的BaCl2溶液,均出现白色沉淀,此沉淀不溶于稀盐酸,经过滤、洗涤、干燥,称量得到的固体质量分别为Xg、Yg,计算SO2+Cl2![]() SO2Cl2反应中,SO2的转化率为_____(用含X、Y的代数式表示)。
SO2Cl2反应中,SO2的转化率为_____(用含X、Y的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置的说法中正确的是
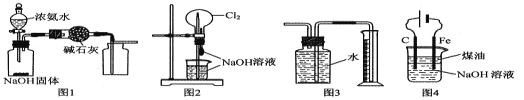
A. 图 1 装置可制取干燥纯净的 NH3
B. 图 2 装置可以完成“喷泉”实验
C. 图 3 装置可测量 Cu 与浓硝酸反应产生气体的体积
D. 图 4 装置可用于实验室制备 Fe (OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 利用丁达尔效应可区分蛋白质溶液与葡萄糖溶液
B. 某物质经科学测定只含有一种元素,则可以断定该物质是一种纯净物
C. 用过滤法无法除去Fe(OH)3胶体中的FeCl3
D. 向豆浆中加入硫酸钙制豆腐,是利用了胶体的聚沉性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列装置完成系列实验,下列说法正确的是( )

A. 铜和浓硝酸的反应与铜和浓硫酸的反应一样需要加热条件下才能进行
B. BaCl2溶液中会出现白色沉淀BaSO3
C. H2S溶液中会出现黄色沉淀,体现了SO2的还原性
D. 为验证碳、硅非金属性的相对强弱,A试管中的试剂可以是KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将X气体通入BaCl2溶液,未见沉淀生成,然后通入Y气体,有沉淀生成,X、Y不可能是( )
A.SO2、H2SB.Cl2、CO2
C.NH3、CO2D.SO2、Cl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com