
| ѡ�� | ʵ����� | ���� | ���� |
| A | պ��Ũ��ˮ�IJ���������ij��Һ | �а��̲��� | ����Һ������Ũ���� |
| B | ��SO2ͨ��Ba��NO3��2��Һ | ������ɫ���� | SO2������Ա��ξ������ɰ�ɫ���� |
| C | ��Zn��ϡ���ᷴӦ����Һ�еμ�����ͭ��Һ | ������������ʼӿ� | ����ͭ���÷�Ӧ�Ĵ��� |
| D | �ò�˿պȡ����ij��Һ������ɫ��Ӧ | ����ʻ�ɫ | ����Һһ����������Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
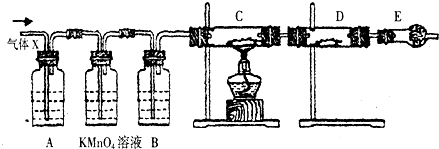
���� A��Ũ��ˮ�ӷ��������ӷ��Ե�Ũ�����Ũ���ᣬ���γɰ��̣�
B����������ͨ�����ᱵ��Һ���γ�ϡ������Һ��������������Ϊ���ᣬ��������ӽ�ϱ������γɳ�����
C��п�ͼ��������ͭ��Ӧ��ͭ������п������ϡ������Һ���γ�ԭ��ط�Ӧ��
D������ʻ�ɫ�����ܲ�������ɫΪ��Ԫ�أ�
��� �⣺A��Ũ��ˮ�ӷ��������ӷ��Ե�Ũ�����Ũ���ᣬ���γɰ��̣�ʵ�����������ͽ��۾���ȷ����A��ȷ��
B����������ͨ�����ᱵ��Һ���γ�ϡ������Һ��������������Ϊ���ᣬ��������ӽ�ϱ������γɳ���������SO2������Ա��ξ������ɰ�ɫ��������B����
C��п�ͼ��������ͭ��Ӧ��ͭ������п������ϡ������Һ���γ�ԭ��ط�Ӧ���ӿ췴Ӧ���ʣ�����ͭ�����Ǹ÷�Ӧ�Ĵ�������C����
D������ʻ�ɫ�����ܲ�������ɫΪ��Ԫ�أ�����Һ��һ����������Һ����D����
��ѡA��
���� ���⿼���˶����������ʵķ����жϣ���Ҫ�����ʵ�����Ӧ�ã����ջ����ǹؼ�����Ŀ�ϼ�


 ��ĩ�óɼ�ϵ�д�
��ĩ�óɼ�ϵ�д� 99��1������ĩ��ѵ��ϵ�д�
99��1������ĩ��ѵ��ϵ�д� ��ǿ��У��ĩ���100��ϵ�д�
��ǿ��У��ĩ���100��ϵ�д� �óɼ�1��1��ĩ���100��ϵ�д�
�óɼ�1��1��ĩ���100��ϵ�д� ��״Ԫ���źþ�ϵ�д�
��״Ԫ���źþ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
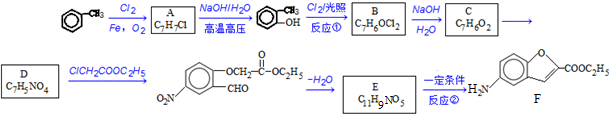
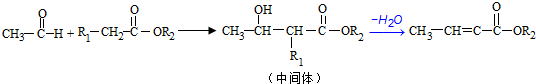
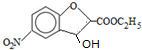 ����Ӧ�ٵķ�Ӧ����Ϊȡ����Ӧ��
����Ӧ�ٵķ�Ӧ����Ϊȡ����Ӧ��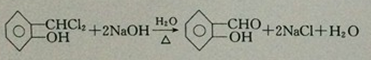 ��ClCH2COOC2H2����������������NaOH��Ӧ���ữ�����л�������ۺϷ�Ӧ�Ļ�ѧ����ʽΪ
��ClCH2COOC2H2����������������NaOH��Ӧ���ữ�����л�������ۺϷ�Ӧ�Ļ�ѧ����ʽΪ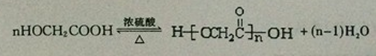 ��
��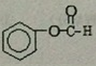 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | Ŀ �� | ���������� |
| A | �Ʊ���ˮFeCl3 | ��FeCl3��Һ�������� |
| B | ��ȥKNO3������NaCl | ��������Ƴ��ȵı�����Һ����ȴ�ᾧ������ |
| C | ֤���ǽ�����Cl��C��Si | ��̼������Һ�м�����������壬��������ͨ������NaHCO3��Һ����ͨ���������Һʱ������ɫ���� |
| D | �ⶨNaCl�л���Na2CO3���� | ȡһ������Ʒ��������ϡ���ᣬ������������ֱ����������ʯ�����գ���������أ�������ԭ��Ʒ��Na2CO3���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | ||
| H2O | C | H2 | CO | |||
| 1 | 650 | 0.01 | 0.02 | 0.008 | 5 | |
| 2 | 800 | 0.02 | 0.03 | 0.017 | 3 | |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | ��ʼ���� | ������ȫ |
| Fe��OH��2 | 7.6 | 9.6 |
| Fe��OH��3 | 2.7 | 3.7 |
| Cu��OH��2 | 4.4 | 8.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H1����H2����H3 | B�� | ��H2����H3��2��H1 | C�� | ��H2����H1����H3 | D�� | ��H3����H2��2��H1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
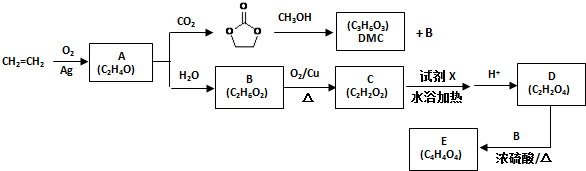
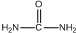 ���ͼ״��ڴ��������������£�����ȡ����Ӧ����DMC����д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ
���ͼ״��ڴ��������������£�����ȡ����Ӧ����DMC����д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ +2CH3OH$��_{��}^{����}$CH3OCOOCH3+2NH3����
+2CH3OH$��_{��}^{����}$CH3OCOOCH3+2NH3�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com