
| 氢化物 | A | B | C | D | E |
| 沸点/℃ | 1317 | 100 | 19.5 | -33 | -162 |

分析 (1)氢化物中,离子晶体的沸点较大,分子晶体中氢化物的沸点随着相对分子质量的增大而增大,但含有氢键的氢化物沸点增大;
(2)图中X原子与周围的4个原子形成正四面体结构,第二、三周期中ⅠA、ⅣA、ⅤA、ⅥA、ⅦA族元素中,金刚石、晶体硅、二氧化硅为原子晶体,且为正四面体向空间延伸的立体网状结构,空间结构为正四面体属于分子晶体且沸点最低的氢化物为CH4,阳离子为正四面体结构为NH4+,铵根离子水解,溶液呈酸性.
解答 解:(1)形成的氢化物有LiH、CH4、NH3、H2O、HF,LiH是离子晶体,CH4、NH3、H2O、HF均形成分子晶体,LiH沸点最大,
故答案为:离子晶体;
(2)第二、三周期中ⅠA、ⅣA、ⅤA、ⅥA、ⅦA族元素中,金刚石、晶体硅、二氧化硅为原子晶体,且为正四面体向空间延伸的立体网状结构,空间结构为正四面体属于分子晶体且沸点最低的氢化物为CH4,阳离子为正四面体结构为NH4+,铵根离子水解:NH4++H2O?NH3.H2O+H+,溶液呈酸性.
故答案为:金刚石、晶体硅;二氧化硅;甲烷;NH4++H2O?NH3.H2O+H+.
点评 本题是对物质结构的考查,涉及晶体类型与熔沸点关系、元素化合物推断、空间构型等,注意识记中学常见晶体结构、微粒空间构型,难度中等.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl2(HCl):饱和食盐水 | B. | H2(H2S、HCl、H2O):碱石灰 | ||
| C. | SO2(HCl):Na2SO3溶液 | D. | CO2(H2S):CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温下,将CH3COONa溶液,盐酸混合后,溶液呈中性,则有c(Cl-)=c(CH3COOH) | |
| B. | 常温下将pH=2的硫酸和pH=12的氨水等体积混合,所得溶液的pH>7 | |
| C. | pH=3的醋酸溶液加水稀释后,溶液中c(CH3COO-)•c(H+)不变 | |
| D. | 向0.1 mol•L-1的Na2SO3溶液中加入少量NaOH固体,c(SO32-)与c(Na+)均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 六方最密堆积是最密堆积,面心立方最密堆积不是最密堆积 | |
| B. | 两者都是最密堆积,其中六方最密堆积是一、三、五…各层球心重合,二、四、六…各层球心重合;面心立方最密堆积是四、五、六…层分别和一、二、三…球心重合 | |
| C. | 原子晶体一般都采用六方最密堆积或面心立方最密堆积 | |
| D. | 只有金属晶体才可能采用六方最密堆积或面心立方最密堆积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
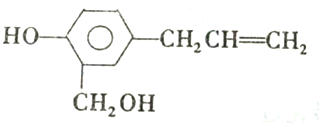 对该物质的性质判断正确的是( )
对该物质的性质判断正确的是( )| A. | 等量A分别与Na和NaOH反应消耗二者的物质的量相同 | |
| B. | 1 mol A 可与2 mol Br2发生取代反应 | |
| C. | A与Na2CO3反应可放出CO2 | |
| D. | 1 mol A 可与4 mol H2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液显酸性 | |
| B. | c(H+)+c(K+)=c(OH-)+c(Cl-)+c(HCO3-)+c(CO32-) | |
| C. | c(Cl-)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | c(K+)>c(HCO3-)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
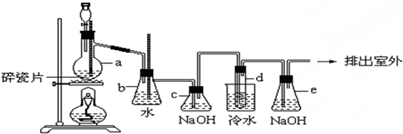
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
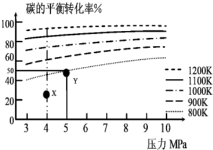 煤气化的一种方法是在气化炉中给煤炭加氢,发生的主要反应为:C(s)+2H2(g)?CH4(g).在VL的容器中投入a mol碳(足量),同时通入a molH2,控制条件使其发生上述反应,实验测得H2的平衡转化率随压力及温度的变化关系如图所示.下列说法正确的是( )
煤气化的一种方法是在气化炉中给煤炭加氢,发生的主要反应为:C(s)+2H2(g)?CH4(g).在VL的容器中投入a mol碳(足量),同时通入a molH2,控制条件使其发生上述反应,实验测得H2的平衡转化率随压力及温度的变化关系如图所示.下列说法正确的是( )| A. | 上述逆反应为吸热反应 | |
| B. | 在5MPa、800K时,该反应的平衡常数为$\frac{V}{a}$ | |
| C. | 在4MPa、1200K时,图中X点υ(H2)正>υ(H2)逆 | |
| D. | 工业上维持6MPa 1000K而不采用10MPa1000K,主要是因为前者氢气的转化率高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | ① | ② | 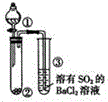 |
| A | 浓氨水 | CaO | |
| B | 浓硝酸 | Cu | |
| C | 浓盐酸 | KMnO4 | |
| D | 浓硫酸 | 蔗糖 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com