
【题目】完成下列各问题
(1)泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,其反应的离子方程式为:________;
(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出①电荷守恒__________________;②物料守恒______________________;③质子守恒______________________________;④下列粒子浓度由大到小的顺序为c(Na+)、c(HCO3-)、c(CO32-),c(H2CO3)、c(OH-)______。
【答案】 3HCO3-+Al3+=Al(OH)3↓+3CO2↑ c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) c(H+)+c(H2CO3)=c(OH-)+c(CO32-) c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-)
【解析】试题分析:本题考查双水解离子方程式的书写,盐溶液中电荷守恒、物料守恒、质子守恒的书写,盐溶液中粒子浓度大小的比较。
(1)Al2(SO4)3属于强酸弱碱盐,由于Al3+的水解Al2(SO4)3溶液呈酸性;NaHCO3溶液中由于HCO3-的水解程度大于电离程度,溶液呈碱性;Al2(SO4)3溶液与NaHCO3溶液混合,由于Al3+、HCO3-水解互相促进,最终Al3+、HCO3-的水解趋于完全生成白色Al(OH)3沉淀和CO2气体,反应的离子方程式为3HCO3-+Al3+=3CO2↑+Al(OH)3↓。
(2)NaHCO3在水溶液中的电离方程式为NaHCO3=Na++HCO3-、HCO3-![]() H++CO32-,在NaHCO3溶液中还存在HCO3-的水解平衡:HCO3-+H2O
H++CO32-,在NaHCO3溶液中还存在HCO3-的水解平衡:HCO3-+H2O![]() H2CO3+OH-和水的电离平衡:H2O
H2CO3+OH-和水的电离平衡:H2O![]() H++OH-。①电荷守恒指溶液中阴离子所带负电荷总数一定等于阳离子所带正电荷总数,电荷守恒为c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)。②物料守恒根据Na、C守恒书写,物料守恒为c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)。③质子守恒指:电解质溶液中,电离、水解等过程中得到的质子(H+)数等于失去的质子(H+)数,对NaHCO3溶液可分析为:
H++OH-。①电荷守恒指溶液中阴离子所带负电荷总数一定等于阳离子所带正电荷总数,电荷守恒为c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)。②物料守恒根据Na、C守恒书写,物料守恒为c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)。③质子守恒指:电解质溶液中,电离、水解等过程中得到的质子(H+)数等于失去的质子(H+)数,对NaHCO3溶液可分析为: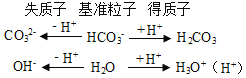 ,质子守恒为c(H+)+c(H2CO3)=c(OH-)+c(CO32-)。④HCO3-的水解程度和电离程度都很微弱,且HCO3-的水解程度大于电离程度,溶液中粒子浓度由大到小的顺序为:c(Na+)> c(HCO3-)> c(OH-)> c(H2CO3)> c(CO32-)。
,质子守恒为c(H+)+c(H2CO3)=c(OH-)+c(CO32-)。④HCO3-的水解程度和电离程度都很微弱,且HCO3-的水解程度大于电离程度,溶液中粒子浓度由大到小的顺序为:c(Na+)> c(HCO3-)> c(OH-)> c(H2CO3)> c(CO32-)。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 常溫常压下,36g18O2中所含的中子数为16NA
B. 4.6 gNO2与N2O4的混合气体中所含氮原子数为0.1 NA
C. 标准状况下,2.24 L 苯含有的分子数等于0.1 NA
D. 在过氧化钠与水的反应中,每消耗0.1mol过氧化钠,转移电子的数目为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的说法,正确的是( )
A.由非金属元素组成的化合物不一定是共价化合物
B.离子化合物可能含共价键,共价化合物可能含离子键
C.任何单质中一定含共价键
D.离子键的本质就是阴阳离子间的静电引力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,某容器装满CO2时总质量为88.8 g,而将此容器装满O2时其总质量为 86.4 g,则此容器的容积为
A.1.12 LB.2.24 LC.3.36LD.4.48 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组同学为了探究“在相同的温度和压强下、相同体积的任何气体都含有相同数目和分子”,他们设计了如下实验装置并记录相关实验数据。实验装置:
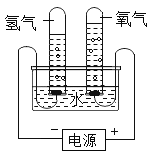
部分实验数据:
温度 | 压强 | 时间 | 水槽中H2O的质量 | H2体积 | O2体积 |
30℃ | 101 kPa | 0 | 300 g | 0 | 0 |
30℃ | 101 kPa | 4分钟 | 298.2 g | 1.243 L |
请回答下列问题:
(1)4分钟时H2、O2物质的量分别是__________mol、___________mol。
(2)该温度下,气体摩尔体积是________________。
(3)假设电解H2O速率相同,2分钟时试管内收集到的H2的体积是___________mL。
(4)根据以上实验得出如下结论,其中不正确的是_________________。
A. 气体摩尔体积与气体的温度相关
B. 在该实验条件下,3 mol O2的气体摩尔体积为74.58 L/mol
C. 同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D. 该实验条件下,O2的密度为1.287 g/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,若Ca(OH)2和CaWO4(钨酸钙)的沉淀溶解平衡曲线如图所示(已知![]() =0.58)。下列分析不正确的是
=0.58)。下列分析不正确的是

A. a点表示Ca(OH)2与CaWO4均未达到溶解平衡状态
B. 饱和Ca(OH)2溶液和饱和CaWO4溶液等体积混合: c(OH-)>c(H+)>c(Ca2+)>c(WO42-)
C. 饱和Ca(OH)2溶液中加入少量Na2O,溶液变浑浊
D. 石灰乳与0.1mol/LNa2WO4溶液混合后发生反应:Ca(OH)2+WO42-=CaWO4+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是来自石油的重要有机化工原料,其产量用来衡量一个国家石油化工发展水平,E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。

(1) A的名称为____;C分子中的官能团名称为_________。
(2)反应③的化学方程式为_________;该反应的反应类型为_________。
(3)反应④的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25℃时,Ksp[Zn(OH)2]=1.0×10-18,Ka(HCOOH)=1.0×10-4。该温度下,下列说法错误的是
A. Zn(OH)2溶于水形成的饱和溶液中c(Zn2+)>1.0×10-6 mol·L-l
B. HCOO-的水解常数为1.0×10-10
C. 向Zn(OH)2悬浊液中加入HCOOH,溶液中c(Zn2+)增大
D. Zn(OH)2+2HCOOH![]() =Zn2++2HCOO-+2H2O的平衡常数K=100
=Zn2++2HCOO-+2H2O的平衡常数K=100
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将H2(g)和I2(g)各0.9 mol的气态混合物充入2 L的密闭容器中,充分反应,5 min后达到平衡,测得c(HI)=0.3 mol/L。(写出计算过程)
(1)计算从反应开始至达到平衡,用H2(g)表示的反应速率________________。
(2)保持温度不变,若向上述容器中充入H2(g)和I2(g)各2 mol,求达到平衡时I2(g)的物质的量浓度___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com