
| A. | 硅的原子结构示意图: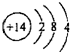 | |
| B. | 乙烯分子比例模型: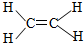 | |
| C. | 二氧化碳分子的电子式: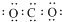 | |
| D. | 硫酸铁的电离方程式:Fe2(SO4)3═2Fe2++3SO42- |
分析 A.硅原子的核电荷数=核外电子总数=14,最外层含有4个电子;
B.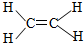 为乙烯的结构式,不是比例模型;
为乙烯的结构式,不是比例模型;
C.二氧化碳分子中含有两个碳氧双键;
D.硫酸铁电离出2个铁离子,不是亚铁离子.
解答 解:A.硅的核电荷数为14,其原子结构示意图为: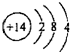 ,故A正确;
,故A正确;
B.C.比例模型需要体现出各原子的相对体积大小,乙烯的比例模型为: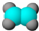 ,故B错误;
,故B错误;
C.二氧化碳分子中含有两个碳氧双键,其正确的电子式为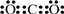 ,故C错误;
,故C错误;
D.硫酸铁为强电解质,在溶液中完全电离,其正确的电离方程式为:Fe2(SO4)3═2Fe3++3SO42-,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、比例模型、原子结构示意图、电离方程式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:选择题
| A. | 2.24 L CO2中含有的原子数为0.3×6.02×1023 | |
| B. | 0.1 mol F- 中含有的电子数等于0.9×6.02×1023 | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 电解饱和食盐水若产生2 g氢气,则转移的电子数目为2×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 夏日的傍晚常常看到万丈霞光穿云而过,美不胜收 | |
| B. | 食品加工厂利用豆浆中加入盐卤做豆腐 | |
| C. | 三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 | |
| D. | 某化工厂利用静电除尘技术去除废气中的固体悬浮物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 我国拥有丰富的海洋资源,海水制盐历史悠久,早在5000年前的仰韶文化时期,先人就利用海水煮盐.为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
我国拥有丰富的海洋资源,海水制盐历史悠久,早在5000年前的仰韶文化时期,先人就利用海水煮盐.为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):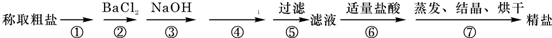
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 制取 聚苯乙烯
制取 聚苯乙烯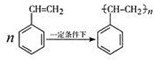
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷和丙烯 | B. | 乙烷和丙烯 | C. | 丙烯和丁炔 | D. | 丁烯和丙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2LN2所含有的分子数为0.5NA | |
| B. | 在标准状况下,22.4 L CO和N2的混合物的物质的量为1mol | |
| C. | 在标准状况下,18g H2O的体积为22.4 L | |
| D. | 1mol SO2中原子数为NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2012年夏,发生在多地的暴雨共造成亿万人受灾.水是组成生命体的重要化学物质,也是一种重要的溶剂,同时也是参与化学反应的重要试剂.怎样利用水为百姓造福将是今后研究的重要课题.请回答下列问题:
2012年夏,发生在多地的暴雨共造成亿万人受灾.水是组成生命体的重要化学物质,也是一种重要的溶剂,同时也是参与化学反应的重要试剂.怎样利用水为百姓造福将是今后研究的重要课题.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com